
 蘇州工匠用白銅打造的食蟹工具“蟹八件”,主要成分是銅鎳合金.Ni能與CO形成正四面體形的配合物Ni(CO)4,CuSO4溶于氨水形成SO4深藍色溶液.
蘇州工匠用白銅打造的食蟹工具“蟹八件”,主要成分是銅鎳合金.Ni能與CO形成正四面體形的配合物Ni(CO)4,CuSO4溶于氨水形成SO4深藍色溶液.分析 (1)Cu是29號元素,原子核外電子數為29,根據核外電子排布規律書寫核外電子排布式;
(2)單鍵為σ鍵,雙鍵含有1個σ鍵,Ni(CO)4分子中含有8個σ鍵;
(3)計算S原子的價電子對數進行判斷;具有相同原子數和價電子數的微粒互稱為等電子體;
(4)由于NH3分子之間存在氫鍵,所以NH3的沸點高于PH3;
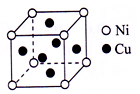
(5)根據均攤法計算晶胞中Ni、Cu原子數目.
解答 解:(1)Cu是29號元素,原子核外電子數為29,基態原子核外電子排布式為:1s22s22p63s23p63d104s1 或3d104s1,
故答案為:ls22s22p63s23p63d104s1 或3d104s1;
(2)分子中存在4個Ni-C鍵,為σ鍵,含有4個C=O鍵,則含有4個σ鍵,共8mol或8×6.02×1023,故答案為:8mol或8×6.02×1023;
(3)SO42-的價電子對數=$\frac{6+2}{2}$=4,形成四條雜化軌道,S原子的雜化方式為sp3,形成四面體結構,價電子對數=孤電子對數+配位原子數,可知孤電子對數為0,所以為正四面體結構;具有相同原子數和價電子數的微粒互稱為等電子體,所以與SO42-互為等電子體的微粒有CCl4等;
故答案為:正四面體;CCl4;
(4)由于NH3分子之間存在氫鍵,所以NH3的沸點高于PH3,
故答案為:高于;NH3分子間存在氫鍵;
(5)晶胞中Ni處于頂點,Cu處于面心,則晶胞中Ni原子數目為8×$\frac{1}{8}$=1、Cu原子數目=6×$\frac{1}{2}$=3,故Cu與Ni原子數目之比為3:1,
故答案為:3:1.
點評 本題考查較為綜合,為高考常見題型,側重考查學生的分析能力的考查,涉及核外電子的排布、分子的空間構型、配位鍵、晶胞的計算等知識點,難度較大,會利用均攤法計算晶胞中含有的離子,注意運用余弦定理計算硫離子和鋅離子之間的距離,為難點.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 電離平衡常數(25℃) | Ka=1.77×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{94}^{238}$Pu與${\;}_{92}^{238}$U互為同位素 | |
| B. | ${\;}_{94}^{238}$Pu與${\;}_{94}^{239}$Pu互為同素異形體 | |
| C. | ${\;}_{94}^{238}$Pu與${\;}_{94}^{239}$Pu具有相同的最外層電子數 | |
| D. | ${\;}_{94}^{238}$Pu與${\;}_{92}^{238}$U具有完全相同的化學性質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 腎功能衰竭等疾病引起的血液中毒,可利用血液透析進行治療,這利用了膠體的滲析原理 | |
| B. | 為防止中秋月餅等富脂食品因被氧化而變質,常在包裝中放入生石灰或硅膠 | |
| C. | 小蘇打是制作饅頭和面包等糕點的膨松劑,還是治療胃酸過多的一種藥劑 | |
| D. | 化工廠可用蘸濃鹽酸的棉棒檢驗輸送氨氣的管道是否漏氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑的大小順序:W>X>Y | |
| B. | W的簡單氣態氫化物的熱穩定性比Y的弱 | |
| C. | Z分別與Q、X形成的化合物中化學鍵類型相同 | |
| D. | X的最高價氧化物對應水化物的堿性在同周期中最強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 14 g乙烯氣體中的氫原子數約為2×6.02×1023 | |
| B. | 標準狀況下,2.24 L H2O含有的共價鍵數約為0.2×6.02×1023 | |
| C. | 1 mol N2與3 mol H2反應生成的NH3分子數約為2×6.02×1023 | |
| D. | 0.1 L 0.5 mol/L CH3COOH溶液中含有的氫離子數約為0.05×6.02×1023 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com