
分析 金屬的腐蝕本質是金屬原子失去電子被氧化的過程;
由于與金屬接觸的介質不同,發生腐蝕的化學原理也不同,一般可分為化學腐蝕和電化學腐蝕,化學腐蝕是指金屬單質直接與氧化性物質反應而被氧化;
電化學腐蝕是形成原電池,被腐蝕金屬做負極,腐蝕速率更快,更普遍.
解答 解:金屬或合金與周圍接觸到的氣體或液體進行化學反應而腐蝕損耗的過程,成為金屬的腐蝕;
金屬單質直接與氧化性物質反應而被氧化發生的腐蝕為化學腐蝕;
形成原電池,被腐蝕金屬做負極,發生氧化反應被腐蝕,為電化學腐蝕;
電化學腐蝕更普遍,腐蝕速率更快;
故答案:金屬或合金與周圍接觸到的氣體或液體進行化學反應而腐蝕損耗的過程;化學腐蝕;電化學腐蝕;電化學腐蝕.
點評 本題考查了化學腐蝕的概念及分類,側重考查學生對基礎知識掌握的熟練程度,題目難度不大,注意對相關知識的記憶.


 一諾書業暑假作業快樂假期云南美術出版社系列答案
一諾書業暑假作業快樂假期云南美術出版社系列答案科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| 摩爾鹽 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子的最外層電子數:X>Y>Z | B. | 單質沸點:Z>Y | ||
| C. | 離子半徑:X2->Y+>Z- | D. | 原子序數:X>Y>Z |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
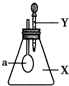 如圖所示,錐形瓶內盛有氣體X,滴管內盛有液體Y.若擠壓膠頭滴管,使液體Y滴入錐形瓶中,振蕩,過一會兒,可見小氣球a鼓脹起來.氣體X和液體Y不可能是( )
如圖所示,錐形瓶內盛有氣體X,滴管內盛有液體Y.若擠壓膠頭滴管,使液體Y滴入錐形瓶中,振蕩,過一會兒,可見小氣球a鼓脹起來.氣體X和液體Y不可能是( )| X | Y | |
| A | NH3 | H2O |
| B | SO2 | NaOH溶液 |
| C | CO2 | 6mol•L-1 H2SO4溶液 |
| D | HCl | 6mol•L-1 Na2SO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 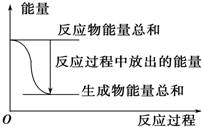 反應過程中能量關系可用如圖表示 | |
| B. | △H的值與反應方程式的計量系數有關 | |
| C. | 若將該反應設計成原電池,鋅為負極 | |
| D. | 若將其設計為原電池,當有32.5 g鋅溶解時,正極放出氣體一定為11.2 L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 化學反應可視為舊鍵斷裂和新鍵形成的過程.化學鍵的鍵能是形成(或拆開)1mol化學鍵時釋放(或吸收)的能量.已知白磷和P4O6的分子結構如下圖所示,現提供以下化學鍵的鍵能(kJ/mol):P-P:198,P-O:360,O=O:498,則反應P4(白磷)+3O2═P4O6的反應熱△H為( )
化學反應可視為舊鍵斷裂和新鍵形成的過程.化學鍵的鍵能是形成(或拆開)1mol化學鍵時釋放(或吸收)的能量.已知白磷和P4O6的分子結構如下圖所示,現提供以下化學鍵的鍵能(kJ/mol):P-P:198,P-O:360,O=O:498,則反應P4(白磷)+3O2═P4O6的反應熱△H為( )| A. | -1 638 kJ/mol | B. | +1 638 kJ/mol | C. | -126 kJ/mol | D. | +126 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | (1) | (2) | ||||||
| 三 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 四 | (10) | (11) | (12) |
 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com