
| A. | 已知2C(s)+O2(g)=2CO(g)△H=-22lkJ/mol,則C的燃燒熱為110.5kJ/mol | |
| B. | 已知C(石墨,s)=C(金剛石,s)△H>0,則金剛石比石墨穩定 | |
| C. | 含20.0gNaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量,則表示該反應中和熱的熱化學方程式為:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4kJ/mol | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)═2CO(g)△H2 則△H1>△H2 |
分析 A.燃燒熱是1mol可燃物完全燃燒生成穩定氧化物時放出的熱量;
B.物質的能量越高越不穩定;
C.依據中和反應實質計算分析,氫氧根離子和氫離子反應是放熱反應;
D.CO燃燒生成二氧化碳還會放出熱量.
解答 解:A.燃燒熱是1mol可燃物完全燃燒生成穩定氧化物時放出的熱量;反應生成的是一氧化碳不是穩定氧化物,不符合燃燒熱概念,故A錯誤;
B.由熱化學方程式可知,石墨總能量小于金剛石,則石墨較穩定,故B錯誤;
C.含20.0g NaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量,則表示該反應中和熱的熱化學方程式為:NaOH(aq)+HCl(aq)=NCl(aq)+H2O(l);△H=-57.3kJ/mol,故C正確;
D.CO燃燒生成二氧化碳還會放出熱量,所以等物質的量的C燃燒生成CO放出熱量比生成二氧化碳放出的熱量少,△H為負值,所以△H1<△H2,故D錯誤;
故選C.
點評 本題考查反應熱及焓變,題目難度中等,本題注意把握熱化學方程式的意義,把握比較反應熱的方法,側重于考查學生的分析能力和計算能力.


 寒假大串聯黃山書社系列答案
寒假大串聯黃山書社系列答案科目:高中化學 來源: 題型:解答題
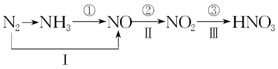 工業上硝酸的制備和自然界中硝酸的生成既有相同的地方,又有區別.線路①、②、③是工業生產硝酸的主要途徑,線路Ⅰ、Ⅱ、Ⅲ是雷電高能固氮過程中硝酸的生成途徑.
工業上硝酸的制備和自然界中硝酸的生成既有相同的地方,又有區別.線路①、②、③是工業生產硝酸的主要途徑,線路Ⅰ、Ⅱ、Ⅲ是雷電高能固氮過程中硝酸的生成途徑.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
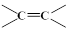 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$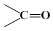 +
+
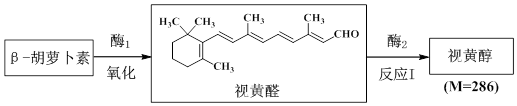
| A. | β-胡蘿卜素的化學式為C40H84 | |
| B. | β-胡蘿卜素在人體吸收時可以用油脂作為相應的溶劑 | |
| C. | 反應I的類型為還原反應 | |
| D. | 許多保健品中都含有β-胡蘿卜素,從其結構推測可能的作用是抗氧化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將 lmolCl2通入到水中,則n(HClO)+n(Cl-)+n(ClO-)=2NA | |
| B. | 常溫常壓下,17g甲基(-14CH3)中所含的中子數為9NA | |
| C. | 含NA個陰離子的Na2O2溶于水形成1L溶液,Na+濃度為1 mol•L-1 | |
| D. | 某溫度時,1LpH=6.5的純水中含有1.0×10-6.5NA個H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
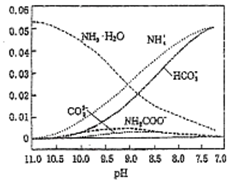 40℃,在氨-水體系中不斷通入CO2,各種離子物質的量濃度隨pH的變化趨勢如圖所示.下列說法正確的是( )
40℃,在氨-水體系中不斷通入CO2,各種離子物質的量濃度隨pH的變化趨勢如圖所示.下列說法正確的是( )| A. | 由圖中數據可計算NH4+的水解平衡常數約為1×10-9 | |
| B. | 不同pH的溶液中存在關系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) | |
| C. | 隨著CO2的通入,$\frac{[O{H}^{-}]}{[N{H}_{3}•{H}_{2}O]}$不斷增大 | |
| D. | 由圖可得離子的水解能力NH4+>HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應過程中既有物質變化又有能量變化,能量的釋放或吸收以物質變化為基礎 | |
| B. | 研究化學反應進行的方向、快慢和限度是化學反應原理的重要內容 | |
| C. | Ag+和Cl-在水溶液中的反應瞬間發生,是因為這類反應活化能接近于零 | |
| D. | 能源就是能提供能量的資源,天然氣、風能、水能都是可再生能源 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 煤的氣化、液化、干餾均有化學變化 | |
| B. | 海水淡化的方法有蒸餾法、電滲析法等 | |
| C. | 天然纖維和合成纖維的主要成分都是纖維素 | |
| D. | “地溝油”經過加工處理可用來制肥皂 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 凡是放熱反應都是自發的,吸熱反應都是非自發的 | |
| B. | 自發反應的熵一定增大,非自發反應的焓一定減小 | |
| C. | 對于熵增反應,若一定溫度下不能自發進行,則該反應的△H>0 | |
| D. | 對于△H>0的反應能自發進行,則該反應的△S<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等質量的硫蒸氣和硫磺分別完全燃燒,二者放出的熱量一樣多 | |
| B. | 氫氣的燃燒熱為 285.8kJ/mol,則氫氣燃燒的熱化學方程式為 2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol | |
| C. | 2H2(g)+O2(g)=2H2O(l)△H=-Q1kJ/mol 2H2(g)+O2(g)=2H2O(g)△H=-Q2kJ/mol,則 Q1>Q2 | |
| D. | 已知中和熱為 57.3 kJ/mol,若將含 0.5molH2SO4的濃溶液與含 1molNaOH 的溶液混合,放出的熱量等于 57.3kJ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com