
| I1/KJ•mol-1 | I2/KJ•mol-1 | I3/KJ•mol-1 | I4/KJ•mol-1 | I5/KJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
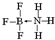 .
.
分析 (1)①Ti是22號元素其原子核外有22個電子,Ti原子失去兩個電子生成Ti2+,該離子核外有1s、2s、2p、3s、3p、3d電子,電子占據的最高能級是3d能級,該能級具有的原子軌道數為5;
②BH4-中B原子價層電子對個數是4且不含孤對電子對,根據價層電子對互斥理論判斷B原子的雜化方式;
(2)①電子層結構相同的離子,離子半徑隨著原子序數增大而減小;
②根據表中數據知,M原子核外有2個電子,位于第IIA族,在化合物中呈現+2價,H為-1價,根據化合價判斷化學鍵;
(3)①結構相似的氫化物,含有氫鍵的物質熔沸點較高;
②NH3容易和分子中有空軌道的BF3反應形成新的化合物,N原子和B原子之間存在配位鍵;
(4)①非極性分子的溶質極易溶于非極性分子的溶劑;
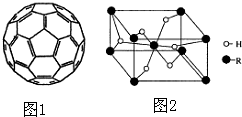
②根據圖知,每個C原子含有σ 鍵個數=$\frac{1}{2}×3$=1.5;
(5)該晶胞中H原子個數=2+4×$\frac{1}{2}$=4,R原子個數=1+8×$\frac{1}{8}$=2,H、R原子個數之比=4:2=2:1;該晶胞體積=$\frac{\frac{M+2}{{N}_{A}}×2}{ρ}$.
解答 解:(1)①Ti是22號元素其原子核外有22個電子,Ti原子失去兩個電子生成Ti2+,所以基態Ti2+中含有的電子數為20;該離子核外有1s、2s、2p、3s、3p、3d電子,電子占據的最高能級是3d能級,該能級具有的原子軌道數為5;
故答案為:20;3d;5;
②BH4-中B原子價層電子對個數是4且不含孤對電子對,根據價層電子對互斥理論知B原子的雜化方式為sp3,
故答案為:sp3;
(2)①電子層結構相同的離子,離子半徑隨著原子序數增大而減小,所以離子半徑:Li+<H-,
故答案為:<;
②根據表中數據知,M原子核外有2個電子,位于第IIA族,在化合物中呈現+2價,為Mg元素,H為-1價,該化合物化學鍵為MgH2,
故答案為:MgH2;
(3)①結構相似的氫化物,含有氫鍵的物質熔沸點較高,氨氣分子和膦分子結構相似,但氨氣中含有氫鍵,導致熔沸點升高,
故答案為:氨氣分子之間可以形成氫鍵;
②NH3容易和分子中有空軌道的BF3反應形成新的化合物,N原子和B原子之間存在配位鍵,其結構式為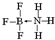 ,
,
故答案為: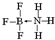 ;
;
(4)①非極性分子的溶質極易溶于非極性分子的溶劑,C60晶體易溶于苯、CS2,C60是非極性分子,故答案為:非極性;
②根據圖知,每個C原子含有σ 鍵個數=$\frac{1}{2}×3$=1.5,1mol該物質中σ 鍵個數=1.5×60×1mol×NA/mol=90NA,故答案為:90NA;
(5)該晶胞中H原子個數=2+4×$\frac{1}{2}$=4,R原子個數=1+8×$\frac{1}{8}$=2,H、R原子個數之比=4:2=2:1,所以其化學式為H2R,該晶胞體積=$\frac{\frac{M+2}{{N}_{A}}×2}{ρ}$cm3=$\frac{2M+4}{a{N}_{A}}$cm3,
故答案為:H2R;$\frac{2M+4}{a{N}_{A}}$.
點評 本題考查物質結構和性質,涉及晶胞計算、相似相溶原理、氫鍵、原子核外電子排布等知識點,這些都是高頻考點,難點是晶胞計算、價層電子對互斥理論,題目難度中等.


科目:高中化學 來源: 題型:解答題
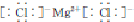 ,工業上用電解無水氯化鎂而不是氧化鎂獲得鎂的原因是消耗大量的電能.
,工業上用電解無水氯化鎂而不是氧化鎂獲得鎂的原因是消耗大量的電能.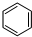 (g)+3H2(g) $?_{FeSO_{4}/Al_{2}O_{3}}^{高溫}$
(g)+3H2(g) $?_{FeSO_{4}/Al_{2}O_{3}}^{高溫}$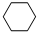 (g)
(g) 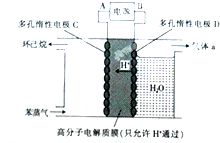
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 亞硫酸鈉有還原性,可用作脫氧劑 | B. | FeCl3有氧化性,可用于制印刷電路 | ||
| C. | 鋁有還原性,可冶煉某些金屬 | D. | 濃硫酸有吸水性,可用于干燥氨氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
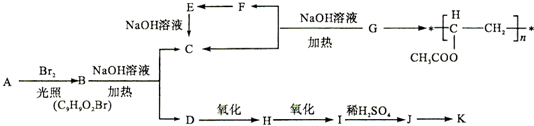
 .
.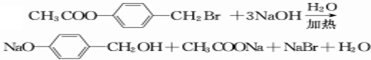 .
.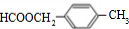 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硫酸具有吸水性,能干燥氫氣,也能干燥氨氣 | |
| B. | 乙醛具有還原性,能被新制氫氧化銅濁液氧化,也能被溴水氧化 | |
| C. | SO2具有漂白性,能使品紅褪色,也能使酸性KMnO4溶液褪色 | |
| D. | 硝酸屬于強酸,能與CaCO3反應生成CO2氣體,也能與CaSO3生成SO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學式 | 電離常數 |
| HF | Ka=3.5×10-4 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| HClO | Ka=3.2×10-8 |
| A. | 同溫同濃度下,溶液的pH值:NaF>NaClO>Na2CO3 | |
| B. | 結合H+的能力:ClO->CO32->F- | |
| C. | 碳酸鈉溶液中加入少量氫氟酸的離子方程式:CO32-+2HF═2F-+H2O+CO2↑ | |
| D. | 次氯酸鈉溶液中通入少量二氧化碳的離子方程式:ClO-+CO2+H2O═HCO3-+HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ZnC2水解生成乙烷(C2H6 ) | B. | Al4C3水解生成丙炔(C3H4) | ||
| C. | Mg2C3水解生成丙炔(C3H4) | D. | Li2C2水解生成乙烯(C2H4) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com