
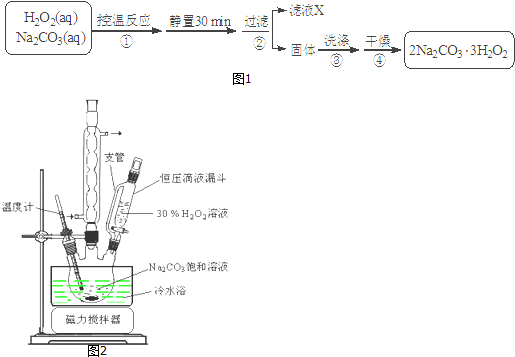
分析 雙氧水和碳酸鈉混合控制溫度發生反應2Na2CO3 (aq)+3H2O2 (aq)?2Na2CO3•3H2O2(s),靜置過濾得到固體2Na2CO3•3H2O2,將固體洗滌、干燥得到較純凈的2Na2CO3•3H2O2;
(1)根據副反應,溫度過高時導致H2O2和過碳酸鈉分解其產率過低,據此分析;
(2)溶液X中含有溶解的過碳酸鈉,鈉離子濃度越大,過碳酸鈉的溶解度越小;
(3)過碳酸鈉難溶于乙醇,水和乙醇互溶;
(4)過碳酸鈉相當于帶結晶雙氧水的碳酸鈉,具有雙氧水和碳酸鈉的性質,強酸、還原性物質易促進過碳酸鈉反應而導致失效;
(5)沉淀法測定過碳酸鈉質量分數需要稱量樣品質量和沉淀質量,列方程計算過碳酸鈉的質量,進而計算得到過碳酸鈉質量分數.
解答 解:(1)制備過碳酸鈉是放熱反應,反應過程中放出的熱量使溫度升高,又根據副反應,溫度過高會導致H2O2和過碳酸鈉分解,從而降低其產率,所以步驟①的關鍵是控制溫度,故答案為:控制溫度;制備過碳酸鈉是放熱反應,防止H2O2和過碳酸鈉分解;
(2)加入氯化鈉固體,鈉離子濃度增大,降低了過碳酸鈉的溶解度,有利于過碳酸鈉的析出,故答案為:增大鈉離子濃度,有利于過碳酸鈉的析出(鹽析作用);
(3)過碳酸鈉難溶于無水乙醇,無水乙醇能和水互溶,且極易揮發,所以選用無水乙醇洗滌的目的是:減少過碳酸鈉的溶解損失,并帶走水分利于干燥,故答案為:減少過碳酸鈉的溶解損失,并帶走水分利于干燥;
(4)過碳酸鈉相當于帶結晶雙氧水的碳酸鈉,具有雙氧水和碳酸鈉的性質,亞硫酸鈉具有還原性與雙氧水反應,HCl具有強酸性可以與碳酸鈉反應,碳酸氫鈉和硅酸鈉都不與過碳酸鈉反應,所以能引起過碳酸鈉失效的是亞硫酸鈉和HCl,故選:BD;
(5)實驗過程中直接測定的物理量為樣品的質量m1g、沉淀的質量m2g,沉淀物質的量=$\frac{m{\;}_{2}g}{197g/mol}$=$\frac{m{\;}_{2}}{197}$mol,設過碳酸鈉物質的量為x,含有的碳酸鈉物質的量為y,
依據碳元素守恒得到:2x+y=$\frac{m{\;}_{2}}{197}$,
由質量可得:314x+106y=m1
解得x=$\frac{m{\;}_{1}-\frac{m{\;}_{2}×106}{197}}{102}$
則過碳酸鈉質量分數為:$\frac{m{\;}_{1}-\frac{m{\;}_{2}×106}{197}}{102}$mol×314g/mol÷m1g=$\frac{314(m{\;}_{1}-\frac{106m{\;}_{2}}{197})}{102m{\;}_{1}}$,
故答案為:樣品的質量m1g、沉淀的質量m2g;$\frac{314(m{\;}_{1}-\frac{106m{\;}_{2}}{197})}{102m{\;}_{1}}$.
點評 本題考查制備實驗方案設計,側重考查分析、計算及知識遷移、基本操作能力,難點是過碳酸鈉質量分數的計算,靈活運用原子守恒解答,(4)利用知識遷移方法解答即可,題目難度中等.


 津橋教育計算小狀元系列答案
津橋教育計算小狀元系列答案科目:高中化學 來源: 題型:解答題

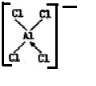 ,[AlCl4]的立體構型名稱為正四面體形.
,[AlCl4]的立體構型名稱為正四面體形.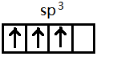 ,鈹與鋁元素性質相近的原因是Be與Al的電負性相近.
,鈹與鋁元素性質相近的原因是Be與Al的電負性相近.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
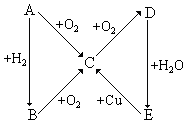 根據如圖所示的A、B、C、D、E五種物質的相互轉化關系,按如下要求填寫相應的物質和有關反應的化學方程式.
根據如圖所示的A、B、C、D、E五種物質的相互轉化關系,按如下要求填寫相應的物質和有關反應的化學方程式.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對于同類型反應,化學平衡常數K的大小反映了化學反應可能進行的程度 | |
| B. | 化學反應速率常數k與濃度無關,但受溫度、催化劑、固體表面性質等因素的影響 | |
| C. | 水的離子積常數Kw、電離平衡常數Ka與溫度有關,不受溶液的酸堿性影響 | |
| D. | 溶度積常數Ksp與難溶電解質的性質和溫度無關,只與沉淀的量有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
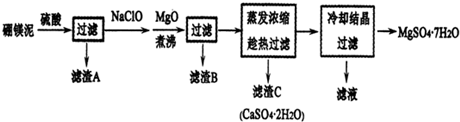
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
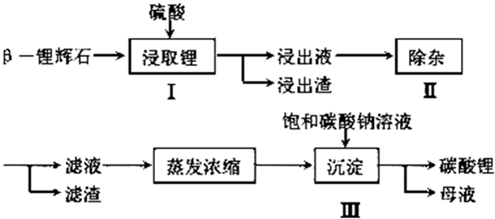
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
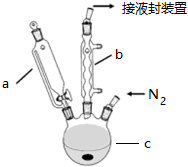
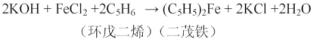
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化 學 鍵 | H-H | I-I |
| 斷開1mol化學鍵時吸收的能量(kJ) | b | c |
| A. | 該反應中反應物的總能量高于生成物的總能量 | |
| B. | 斷開1 mol H-H 鍵和1 mol I-I 鍵所需能量大于斷開2 mol H-I 鍵所需能量 | |
| C. | 斷開2 mol H-I鍵所需能量為(a+b+c)kJ | |
| D. | 向密閉容器中加入2 mol H2和2 mol I2,充分反應后放出的熱量小于2a kJ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com