
| A. | 100 mL | B. | 200 mL | C. | 300 mL | D. | 400 mL |
分析 金屬失去的電子等于氧氣與混合氣體反應生成硝酸獲得的電子,向所得硝酸鹽溶液中加入4mol/LNaOH溶液至沉淀最多停止加入,此時溶液為硝酸鈉溶液.根據硝酸根守恒可知,鈉離子物質的量等于金屬失去的電子的物質的量.據此計算NaOH的物質的量,進而計算溶液的體積.
解答 解:標準狀況下3.36L氧氣的物質的量=$\frac{3.36L}{22.4L/mol}$=0.15mol,所以氧氣獲得電子的物質的量為0.15mol×4=0.6mol;
金屬失去的電子等于氧氣與混合氣體反應生成硝酸獲得的電子,為0.6mol,
向所得硝酸鹽溶液中加入2mol/LNaOH溶液至沉淀最多停止加入,此時溶液為硝酸鈉溶液.根據硝酸根離子守恒可知,鈉離子物質的量等于金屬失去的電子的物質的量為0.6mol.則NaOH為0.6mol,所以V(NaOH)=$\frac{0.6mol}{2mol/L}$=0.3L=300mL.
故選:C.
點評 本題考查了氧化還原反應的有關計算,如果利用常規方考慮每個細節的反應將無法解答,根據守恒思想來從總體上分析,再結合轉移電子守恒、原子守恒解答,題目難度較大,注意守恒思想的運用.


 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案科目:高中化學 來源: 題型:解答題
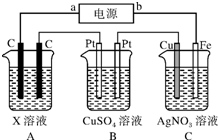 如圖所示,電解一段時間后,測得C中Ag+減少了0.1mol,Fe電極被溶解.試回答:
如圖所示,電解一段時間后,測得C中Ag+減少了0.1mol,Fe電極被溶解.試回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
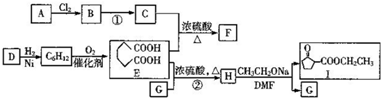
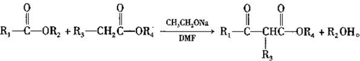
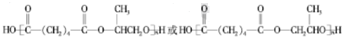 ,1中官能團的名稱酯基和羰基.
,1中官能團的名稱酯基和羰基.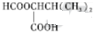 .
.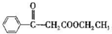 寫出合成路線圖.
寫出合成路線圖.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:C>A | |
| B. | 離子半徑:D3+>B2- | |
| C. | 非金屬性:A>B | |
| D. | 最高價氧化物對應水化物的堿性:C<D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
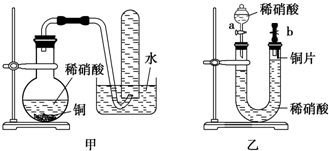
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用雙氧水代替高錳酸鉀制氧氣 | |
| B. | 用多量的氯氣進行性質實驗 | |
| C. | 用溴水代替碘水進行萃取實驗 | |
| D. | 用銅粉代替銅絲進行銅和濃硝酸的反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com