
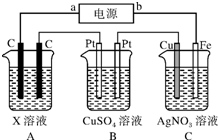
 如圖所示,電解一段時間后,測得C中Ag+減少了0.1mol,Fe電極被溶解.試回答:
如圖所示,電解一段時間后,測得C中Ag+減少了0.1mol,Fe電極被溶解.試回答:分析 (1)有外接電源,都是電解池,C中Fe電極溶解,則C作陽極,與陽極相連的是電源的正極;
(2)根據電子轉移守恒計算B中銅離子的物質的量,再根據公式c=$\frac{n}{V}$計算;根據析出什么加什么的原則分析;
(3)C中Ag+減少了0.1mol,轉移電子0.1mol,鹽酸溶液中是氫離子和氯離子放電產生氫氣和氯氣,根據電極反應關系式計算氣體總體積;計算溶液中剩下氫離子濃度得出PH.
解答 解:(1)圖中有外接電源,都是電解池,C中Fe電極溶解,則C作陽極,陽極鐵失電子發生氧化反應,電極反應為Fe-2e-═Fe2+,與陽極相連的是電源的正極,故答案為:正;Fe-2e-═Fe2+;
(2)當C中Ag+減少0.1mol時,轉移電子0.1mol,B中Cu2+恰好完全析出為Cu,電極反應為:Cu2++2e-═Cu,則B中銅離子的物質的量為$\frac{0.1mol}{2}$=0.05mol,溶液中硫酸銅的c=$\frac{n}{V}$=$\frac{0.05mol}{0.1L}$=0.5mol/L,電解硫酸銅溶液的總反應為:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2 ↑+4H+,析出銅和氧氣,要使溶液復原則可加氧化銅和碳酸銅,氧化銅與氫離子反應生成銅離子和水,碳酸銅與氫離子反應生成銅離子和水,二氧化碳溢出,
故答案為:0.5mol/L;CuO或CuCO3;
(3)C中Ag+減少了0.1mol,轉移電子0.1mol,鹽酸溶液中是氫離子和氯離子放電產生氫氣和氯氣,100mL 1.1mol/L的HCl溶液中氫離子物質的量為0.11mol,鹽酸過量,2H+~H2~2e-,Cl2~2e-,則產生的氣體有$\frac{0.1mol}{2}$$+\frac{0.1mol}{2}$=0.1mol,在標準狀況下的總體積為0.1mol×22.4L/mol=2.24L;此時溶液中剩下氫離子物質的量為0.11mol-0.1mol=0.01mol,氫離子的濃度為0.01mol÷0.1L=0.1mol/L,PH=1,
故答案為:2.24L;1.
點評 本題以電解原理為載體考查了電極反應式的書寫、離子濃度的計算,難度不大,利用電子轉移守恒計算是解題的關鍵.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ;
; ;
; ;
; ;
; ;
; ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 明礬凈水 | |
| B. | 使用熱的純堿溶液去除油污 | |
| C. | 實驗室配制FeCl3溶液時加入少量稀鹽酸 | |
| D. | 實驗室制氫氣時加入CuSO4可加快反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 聚乙烯塑料制品可用于食品的包裝 | |
| B. | 石油催化裂化的主要目的是提高汽油等輕質油的產量與質量 | |
| C. | 原電池放電發生化學變化,同時能量發生轉化 | |
| D. | 開發太陽能,推廣使用甲醇汽油,使用無磷洗滌劑都可直接降低碳排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室用Zn和稀硝酸制取H2:Zn+2H+═Zn2++H2↑ | |
| B. | H2SO4溶液中和Ba(OH)2溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| C. | 向Ca(HCO3)2溶液中加入過量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向苯酚鈉溶液中通入少量的CO2:2C4H3O-+CO2+H2O═2C6H5OH+CO3-2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 100 mL | B. | 200 mL | C. | 300 mL | D. | 400 mL |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com