
| 物質 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸點/℃ | 57.7 | 12.8 | | 315 | |
| 熔點/℃ | -70.0 | -107.2 | | | |
| 升華溫度/℃ | 180 | 300 | 162 |
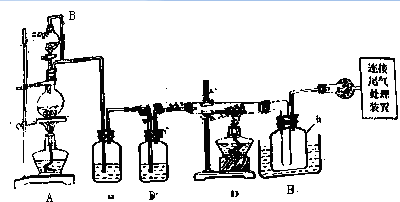
分析 由制備四氯化硅的實驗流程可知,A中發生二氧化錳與濃鹽酸的反應生成氯氣,B中飽和食鹽水除去HCl,C裝置中濃硫酸干燥氯氣,D中發生Si與氯氣的反應生成四氯化硅,由信息可知,E裝置制取氫氣,F可防止倒吸,最后氫氣還原SiCl4,
(1)裝置A中g管使分液漏斗和燒瓶連通;裝置C中的試劑應該吸收水而不能吸收氯氣;產物SiCl4沸點低;
(2)D中氯氣與粗硅反應生成SiCl4,h瓶收集粗產物,精餾粗產品可得高純度四氯化硅,由表中數據可以看出,蒸出SiCl4氣體時,BCl3早已成氣體被蒸出,而AlCl3、FeCl3、PCl5升華溫度均低于SiCl4.
解答 解:由制備四氯化硅的實驗流程可知,A中發生二氧化錳與濃鹽酸的反應生成氯氣,B中飽和食鹽水除去HCl,C裝置中濃硫酸干燥氯氣,D中發生Si與氯氣的反應生成四氯化硅,由信息可知,E裝置制取氫氣,F可防止倒吸,最后氫氣還原SiCl4,
(1)濃鹽酸有揮發性,故分液漏斗要加蓋,加蓋后如沒有g管,則鹽酸就不易流下去,g管的作用是平衡壓強,使液體順利流出并防止漏氣;制得的氯氣中含有氯化氫和水,裝置B用飽和食鹽水除去氯化氫,裝置C用濃硫酸吸水;產物SiCl4沸點低,需要冷凝收集,
故答案為:平衡壓強;濃硫酸;使SiCl4冷凝收集;
(2)D中氯氣與粗硅反應生成SiCl4,h瓶收集粗產物,精餾粗產品可得高純度四氯化硅,由表中數據可以看出,蒸出SiCl4氣體時,BCl3早已成氣體被蒸出,而AlCl3、FeCl3、PCl5升華溫度均低于SiCl4,所以當SiCl4蒸出后,而AlCl3、FeCl3、PCl5還為固體留在瓶里,
故答案為:Al、P.
點評 本題考查制備實驗方案的設計,綜合了氯氣的制法、硅的提純等實驗知識,注意把握制備原理及實驗流程中的反應、物質的性質等為解答的關鍵,側重分析與實驗能力的綜合考查,題目難度中等.


 怎樣學好牛津英語系列答案
怎樣學好牛津英語系列答案科目:高中化學 來源: 題型:選擇題
| A. | 常溫下氯氣與燒堿溶液反應:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | AlCl3溶液中加入過量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 金屬鈉與水反應:Na+H2O═Na++OH-+H2↑ | |
| D. | 銅與稀硝酸反應:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 氫氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有在生物體內才能合成的物質 | B. | 有機物都是含有碳元素的化合物 | ||
| C. | 有機化合物都能燃燒 | D. | 含有碳元素的物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu$→_{v}^{O_{2}}$CuO$\stackrel{H_{2}SO_{4}}{→}$CuSO4溶液$\stackrel{結晶}{→}$CuSO4•5H2O | |
| B. | Al$→_{v}^{O_{2}}$Al2O3$\stackrel{{H}_{2}S{O}_{4}}{→}$Al2(SO4)3溶液$\stackrel{加熱蒸干}{→}$Al2(SO4)3 | |
| C. | FeSO4溶液$\stackrel{{H}_{2}S}{→}$FeS$→_{干燥}^{過濾}$FeS晶體 | |
| D. | MgCl2溶液$→_{過濾}^{NH_{3}}$Mg(OH)2$\stackrel{適量HN{O}_{3}}{→}$Mg(NO3)2溶液$\stackrel{結晶}{→}$Mg(NO3)•6H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 )的廢水可以通過構成微生物電池除去,其原理如圖所示.
)的廢水可以通過構成微生物電池除去,其原理如圖所示.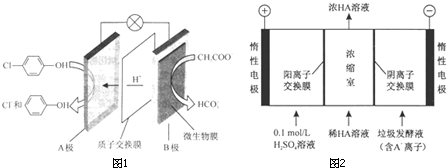
 -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-.
-OH+Cl-.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溴乙烷與NaOH水溶液混合加熱后,經冷卻,加入硝酸銀溶液有淡黃色沉淀 | |
| B. | 淀粉在硫酸作用下水解得到葡萄糖,再加入新制銀氨溶液并水浴加熱,可得銀鏡 | |
| C. | 檢驗溴乙烷消去產物中的乙烯,可將反應逸出的氣體直接通入酸性KMnO4溶液中 | |
| D. | 通過核磁共振氫譜的方法,可以檢驗出溴乙烷在NaOH水溶液中水解的產物有乙醇生成 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com