
分析 (1)依據用濃溶液配制一定物質的量濃度稀溶液一般步驟選擇需要的儀器;
(2)①A.先計算濃硫酸的物質的量濃度,然后根據稀釋過程中硫酸的物質的量不變進行計算需要濃硫酸溶液的體積;
E.依據定容的正確操作解答;
②用濃溶液配制一定物質的量濃度稀溶液一般步驟:計算、量取、稀釋、移液、洗滌、定容、搖勻等,據此排序;
③依據濃硫酸體積選擇合適規格的容量瓶;
④如果對裝有濃硫酸的量筒仰視讀數,導致量取濃硫酸體積偏大,依據C=$\frac{n}{V}$進行誤差分析;
⑤容量瓶不能盛放過熱液體,所以移液前,應進行冷卻.
解答 解:(1)用濃溶液配制一定物質的量濃度稀溶液一般步驟:計算、量取、稀釋、移液、洗滌、定容、搖勻等,用到的儀器:量筒、膠頭滴管、燒杯、玻璃棒、容量瓶,配制100mL物質的量濃度為1mol/L的稀硫酸需要100mL容量瓶;所以還缺少的儀器:100ml容量瓶、膠頭滴管;
故答案為:100ml容量瓶、膠頭滴管;
(2)①A.質量分數為98%,密度為1.84g•cm-3的濃硫酸物質的量濃度C=$\frac{1000ρω}{M}$=$\frac{1000×1.84×98%}{98}$=18.4mol/L,
設需要濃硫酸體積V,則依據稀釋過程中硫酸的物質的量不變得:V×18.4mol/L=1mol/L×100mL,解得V=5.4mL;
故答案為:5.4;
E.定容時,將蒸餾水直接加入容量瓶,至液面接近刻度線1-2cm,改用膠頭滴管逐滴滴加到凹液面與刻度線相切;
故答案為:1-2cm;
②用濃溶液配制一定物質的量濃度稀溶液一般步驟:計算、量取、稀釋、移液、洗滌、定容、搖勻等,所以正確的操作順序為:DACBEGF;
故答案為:DACBEGF;
③依據A可知需要濃硫酸體積為5.4mL,所以應選擇10mL量筒,
故選A;
④如果對裝有濃硫酸的量筒仰視讀數,導致量取濃硫酸體積偏大,則溶質的物質的量偏大,溶液濃度偏高;
故答案為:偏高;
⑤容量瓶不能盛放過熱液體,而濃硫酸稀釋產生大量的熱,所以移液前,應冷卻到室溫;
故答案為:冷卻至室溫.
點評 本題考查了一定物質的量濃度溶液的配制,明確配制原理及操作步驟是解題關鍵,注意誤差分析的方法和技巧,題目難度不大.


科目:高中化學 來源: 題型:解答題
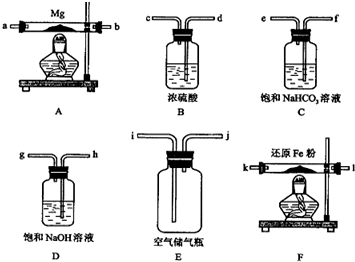
| 裝置 | 目的 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
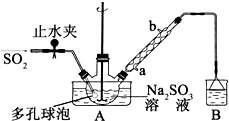 次硫酸氫鈉甲醛(NaHSO2•HCHO•2H2O)俗稱吊白塊,不穩定,120℃時會分解.在印染、醫藥以及原子能工業中有廣泛應用.以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如下:
次硫酸氫鈉甲醛(NaHSO2•HCHO•2H2O)俗稱吊白塊,不穩定,120℃時會分解.在印染、醫藥以及原子能工業中有廣泛應用.以Na2SO3、SO2、HCHO和鋅粉為原料制備次硫酸氫鈉甲醛的實驗步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 平衡時c(NH3)=5mol/L | |
| B. | 平衡時HI分解率為20% | |
| C. | 混合氣體的平均摩爾質量不再發生變化不可以作為判斷該反應達到平衡狀態的標志 | |
| D. | 平衡后縮小容器體積,NH4I的物質的量增加,I2的物質的量不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸銨在室溫下能自發發生分解,是由于反應生成了易揮發的氣體,使體系的熵增大 | |
| B. | 同一種物質氣態時熵值最大,液態時次之,而固態時熵值最小 | |
| C. | 與外界隔離的體系,自發過程將導致體系的熵減小 | |
| D. | 在一定條件下,非自發進行的反應也能夠發生 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
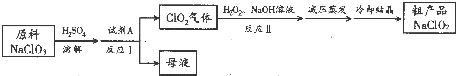
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 用物質A表示2 s內的平均反應速率為0.3 mol/(L•s) | |
| B. | 用物質B表示2s內的平均反應速率為0.6 mol/(L•s) | |
| C. | 2 s后物質B的濃度為0.35 mol/L | |
| D. | 2 s后物質A的轉化率為30% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可用丁達爾效應區分溶液和膠體 | |
| B. | 將1.0molFeCl3全部制成膠體,其中氫氧化鐵膠粒為NA個 | |
| C. | Fe(OH)3膠體的電泳實驗說明了膠體粒子帶有電荷 | |
| D. | 江河入海口三角洲的形成,通常與膠體的性質有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 左盤高 | B. | 右盤高 | C. | 仍保持平衡 | D. | 不能確定 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com