
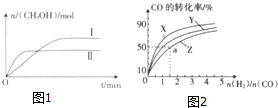
 在一定體積的密閉容器中,通入一定量的CO2和H2,在兩種溫度下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),測得CH3OH的物質的量隨時間的變化如圖1.
在一定體積的密閉容器中,通入一定量的CO2和H2,在兩種溫度下發生反應:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),測得CH3OH的物質的量隨時間的變化如圖1.| 容器 | 甲 | 乙 |
| 反應物投入量 | 1molCO2,3mol H2 | 2mol CO2,6mol H2 |
分析 (1)II平衡時間小于I,說明II反應速率大于I,且平衡時II中CH3OH的物質的量小于I,說明平衡向逆反應方向移動,則只能是升高溫度,溫度越高,化學平衡常數越小;
(2)①該反應為氣體體積減小的反應,體積相同,乙中各反應物的起始物質的量是甲的2倍,壓強乙大于甲,據此判斷;
②根據甲中平衡后氣體的壓強為開始的0.8倍,可計算得甲中平衡時CH3OH(g)的濃度,乙中CH3OH(g)的濃度大于甲中兩倍,據此判斷;
(3)根據正逆反應速率相等,組成成分不變,以及反應前后氣體體積變化的可逆反應中的壓強等判斷反應是否平衡;
(4)化學平衡常數等于生成物濃度的系數次冪之積除以反應物濃度的系數次冪之積,該反應是放熱反應,根據溫度對平衡的影響判斷曲線;可逆反應不能完全正向進行,據此判斷反應熱.
解答 解:(1)II平衡時間小于I,說明II反應速率大于I,且平衡時II中CH3OH的物質的量小于I,說明平衡向逆反應方向移動,則只能是升高溫度,即II的溫度大于I,溫度越高,平衡向逆反應方向移動,導致化學平衡常數越小,所以KⅠ>KⅡ,
故答案為:>;
(2)①該反應為氣體體積減小的反應,體積相同,乙中各反應物的起始物質的量是甲的2倍,壓強乙大于甲,所以反應乙正向進行的程度大于反應甲,所以P乙<2p甲,
故選c;
②在甲容器中,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),
起始(mol) 1 3 0 0
轉化(mol) x 3x x x
平衡(mol) 1-x 3-3x x x
根據甲中平衡后氣體的壓強為開始的0.8倍,可得 1-x+3-3x+x+x=0.8×(3+1),x=0.4,所以CH3OH的物質的量為0.4mol,乙中的壓強大于甲,平衡向正反應方向移動,且乙的起始物質的量是甲的兩倍,所以乙中CH3OH(g)的濃度大于甲中兩倍,
故選b;
(3)a.此反應若在恒壓容器中進行,所以當容器中壓強不變時,所以不能說明反應處于平衡狀態;
b.H2的體積分數不變時,反應處于平衡狀態;
c.c(H2)=3c(CH3OH),未說明是正反應還是逆反應,所以不能說明反應處于平衡狀態;
d.此反應若在恒壓容器中進行,反應前后容器體積發生變化,氣體質量不變,所以容器中密度不變時,說明反應處于平衡狀態;
e.2個C=O斷裂的同時有3個H-H斷裂,都是指的正反應速率,所以不能說明反應處于平衡狀態;
故選bd;
根據正逆反應速率相等,組成成分不變,以及反應前后氣體體積變化的可逆反應中的壓強等判斷反應是否平衡;
(4)化學平衡常數等于生成物濃度的系數次冪之積除以反應物濃度的系數次冪之積,根據CO(g)+2H2(g)?CH3OH(g)可得K=$\frac{c(C{H}_{3}OH)}{c(CO)•{c}^{2}({H}_{2})}$,該反應是放熱反應,升高溫度平衡逆向移動,CO的轉化率下降,Z線對應的CO的轉化率最低,所以對應的溫度為270℃,可逆反應不能完全正向進行,所以1molCO反應放出的熱量最多為90.8kJ,
故答案為:$\frac{c(C{H}_{3}OH)}{c(CO)•{c}^{2}({H}_{2})}$;270℃;90.8.
點評 本題綜合性考查了影響平衡移動的因素、平衡常數的表達式及平衡狀態的判斷等,側重于對基礎知識的綜合應用的考查,題目難度中等,側重于考查學生的分析能力和解決問題的能力.


科目:高中化學 來源: 題型:解答題
 在某密閉容器中進行 以下反應:M(g)+N(g)?R(g)+2L(?),且此反應符合如圖所示圖象.圖中R%表示R在平衡混合物中的含量,T1、T2表示體系溫度,P1、P2表示體系壓強.請判斷
在某密閉容器中進行 以下反應:M(g)+N(g)?R(g)+2L(?),且此反應符合如圖所示圖象.圖中R%表示R在平衡混合物中的含量,T1、T2表示體系溫度,P1、P2表示體系壓強.請判斷查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫有三種核素:H、D、T | B. | S2-的結構示意圖: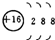 | ||
| C. | 石英中存在SiO2分子 | D. | CO2分子的結構式:O=C=O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18.8g苯酚中含有碳碳雙鍵的個數為0.6NA | |
| B. | 17g羥基(-OH)所含有的電子數是10NA | |
| C. | 標準狀況下,11.2L 三氯甲烷所含分子數為0.5NA | |
| D. | 常溫常壓下,3.0g葡萄糖和冰醋酸的混合物中含有的原子總數為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 )曾入選倫敦奧運會指定產品,下面是工業合成龍葵醛的路線圖(部分反應條件及副產物已略去),回答問題:
)曾入選倫敦奧運會指定產品,下面是工業合成龍葵醛的路線圖(部分反應條件及副產物已略去),回答問題: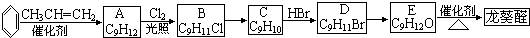
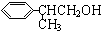 +O2
+O2
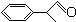 +2H2O.
+2H2O. 、
、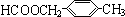 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| B. | 棉、麻、絲、毛及合成纖維完全燃燒都只生成CO2和H2O | |
| C. | 植物油和裂化汽油可用溴水鑒別 | |
| D. | 在雞蛋白溶液中加入濃HNO3,微熱后會生成黃色物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
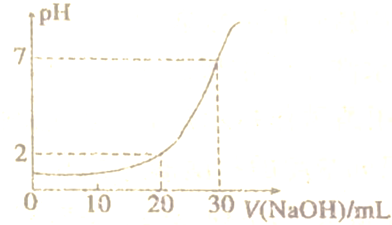
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 濃度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常用鋁鹽溶液與氨水反應制取氫氧化鋁 | |
| B. | 澄清石灰水盛裝在用玻璃塞塞緊的試劑瓶中 | |
| C. | 氫氣在氯氣中燃燒產生蒼白色火焰 | |
| D. | 新制氯水通常保存在棕色試劑瓶 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com