
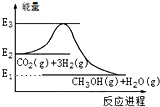
| A. | E2_E1是該反應的熱效應 | |
| B. | E3_E1是該反應的熱效應 | |
| C. | 該反應放熱,在常溫常壓下就能進行 | |
| D. | 實現變廢為寶,且有效控制溫室效應 |
分析 A、根據化學反應的焓變等于反應物和產物的能量之差來回答;
B、根據化學反應的焓變等于反應物和產物的能量之差來回答;
C、根據反應物和產物能量的高低來確定反應的吸放熱情況;
D、二氧化碳是溫室氣體,甲醇可以做燃料,據此回答.
解答 解:A、化學反應的熱效應等于反應物和產物的能量之差,反應反應物的能量高于產物能量,所以反應放熱,所以反應的熱效應是E1_E2,故A錯誤;
B、化學反應的熱效應等于反應物和產物的能量之差,所以反應的熱效應是E1_E2,故B錯誤;
C、該反應反應物的能量高于產物能量,所以反應放熱,但是放熱反應在常溫常壓下不一定就能進行,故C錯誤;
D、二氧化碳是溫室氣體,甲醇可以做燃料,二氧化碳和氫氣轉化為甲醇和水的反應可以反應可以實現變廢為寶,且有效控制溫室,故D正確.
故選D.
點評 本題考查學生反應熱的判斷和計算知識,注意圖象內容的理解和把握是關鍵,難度中等.


 奪冠金卷全能練考系列答案
奪冠金卷全能練考系列答案科目:高中化學 來源: 題型:選擇題
| A. | 乙烯使溴水、高錳酸鉀溶液褪色 | |
| B. | 碘片、氯化銨晶體受熱消失 | |
| C. | 二氧化硫和氯氣使品紅溶液褪色 | |
| D. | 乙醛、葡萄糖與銀氨溶液水浴加熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 酸 | 電離常數K1 | 電離常數K2 |
| H2SO3 | 1.54×10-2 | 1.02×10-7 |
| H2CO3 | 4.3×10-7 | 5.6×10-11 |
| A. | pH:Na2CO3溶液小于Na2SO3溶液 | |
| B. | 結合H+能力:CO32-弱于SO32- | |
| C. | NaHSO3溶液顯酸性的原因是:NaHSO3═Na++H++SO32- | |
| D. | ①與②溶液等體積混合后的溶液中:c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 氮元素只被氧化 | |
| B. | 豆科植物根瘤菌固氮屬于自然固氮 | |
| C. | 其它元素也參與了氮循環 | |
| D. | 含氮無機物和含氮有機物可相互轉化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 某稀硫酸和稀硝酸混合溶液100mL,逐漸加入鐵粉,產生氣體的量隨鐵粉加入量的變化如圖所示.下列說法錯誤的是( )
某稀硫酸和稀硝酸混合溶液100mL,逐漸加入鐵粉,產生氣體的量隨鐵粉加入量的變化如圖所示.下列說法錯誤的是( )| A. | H2SO4濃度為4mol/L | B. | 溶液中最終溶質為FeSO4 | ||
| C. | 原混合酸中NO3-濃度為0.2mol/L | D. | AB段反應為:Fe+2Fe3+→3Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向兩種氣體中加入適量水,震蕩 | B. | 將兩種氣體分別通入AgNO3溶液中 | ||
| C. | 用濕潤的淀粉KI試紙檢驗 | D. | 將兩種氣體加壓、冷卻 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 29g•mol-1 | B. | 29g | C. | 58g•mol-1 | D. | 58g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
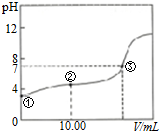
| A. | 兩溶液反應的離子方程式是H++OH-+H2O | |
| B. | 圖中②點所示溶液中:2c(Na+)=c(HA)+c(A-) | |
| C. | 圖中②點所示溶液中:c(A-)>c(H+)>c(HA)>c(OH-) | |
| D. | 圖中③點所示滴入的NaOH溶液的體積V=20.00mL |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com