
| ��(sh��)�(y��n)��̖(h��o) | 1 | 2 | 3 | 4 |
| ����NaOH��Һ���w�e��mL�� | 20.05 | 20.00 | 18.80 | 19.95 |
���� ��1��pH=-lgc��H+���������ͬ����ҺpH��С����Һ�К��x�ӝ�ȴ�С����Ӌ(j��)���Дࣻ
��2����Һ�����|(zh��)���|(zh��)������ͬ�r(sh��)���c�A����(y��ng)����Һ�����ԣ������Ƕ�Ԫ�ᣬ��������������Дࣻ
��3��pH��ͬ��Һ�К��x�ӝ����ͬ������(j��)������}��鏊(qi��ng)�ᣬ��Һ����ȫ��x���������늽��|(zh��)����Һ�в�����x������
��4�����к͵ζ��Č�(sh��)�(y��n)���?y��n)飺�z�顢ϴ�졢��(r��n)ϴ���bҺ���x��(sh��)��ȡ���y(c��)Һ����ָʾ�����ζ����x��(sh��)��̎��UҺ��ϴ�죻
�ڵζ��^(gu��)���У��۾�עҕ���F��ƿ?j��)?n��i)��Һ�ɫ��׃�����M(j��n)�еζ��K�c(di��n)�Дࣻ
��3�ε��w�e�`���^����ȥ����(j��)���Ό�(sh��)�(y��n)��ƽ��ֵ������Ø�(bi��o)��(zh��n)Һ���w�e���ٓ�(j��)c��HCl��=$\frac{c��NaOH��V��NaOH��}{V��HCl��}$���㣻
��5����A�к͵ζ��е��`���������Ҫ���e(cu��)�`������(du��)��(bi��o)��(zh��n)ҺV��NaOH����Ӱ푣��e(cu��)�`������(d��o)��(bi��o)��(zh��n)Һ�w�eƫ�t�y(c��)���Y(ji��)��ƫ�ߣ��e(cu��)�`������(d��o)��(bi��o)��(zh��n)Һ�w�eƫС���t�y(c��)���Y(ji��)��ƫ�ͣ���(j��)�˷�����
��� �⣺��1����(d��ng)����pH��ͬ�r(sh��)����Һ�К��x�ӝ����ͬ�����O(sh��)�ṩ1mol/L�Ě��x�ӣ���Ҫ�����ȑ�(y��ng)����1mol/L����Ҫ�Ȼ�����Һ��Ȟ�1mol/L����ҪH2SO4 ��Һ��Ȟ�0.5mol/L�������|(zh��)��������ɴ�С���е��ǣ��٣��ڣ��ۣ�
�ʴ𰸞飺A��
��2���w�e�͝����ͬ�Ģ١��ڡ�������Һ�����O(sh��)���|(zh��)��1mol���քe�cͬ��ȵğ��A��Һ����(y��ng)��Ҫʹ����(y��ng)����Һ��pH��7����CH3COOH�����ᣬǡ���к����ɴ����c��Һ�ʉA�ԣ�������Ҫ���AС��1mol�����Ȼ����1mol�������cǡ�÷���(y��ng)��Һ�����ԣ���1molH2SO4��2molǡ�÷���(y��ng)��Ҫ?d��)������c2mol�� ������A��Һ���w�e�ɴ�С�P(gu��n)ϵ�飺�ۣ��ڣ��٣�
�ʴ𰸞飺B��
��3����(d��ng)������pH��ͬ�w�e��ͬ�r(sh��)��ͬ�r(sh��)���������\�����a(ch��n)����ͬ�w�e�Ě��w����ͬ��r����������}��鏊(qi��ng)�ᣬPH��ͬ����Һ�К��x�ӝ����ȣ������c�\����(y��ng)���ɚ���������ȣ���=��=�ۣ���������Һ�К��x�ӝ�ȜpС���������x�̶�������˴�����Һ�Юa(ch��n)�����ķ���(y��ng)���ʴ���������}������ʣ����Է���(y��ng)���ɚ��w���w�e�飺�٣���=��
�ʴ𰸞飺C��E��
��4�����к͵ζ��Č�(sh��)�(y��n)���?y��n)飺�z�顢ϴ�졢��(r��n)ϴ���bҺ���x��(sh��)��ȡ���y(c��)Һ����ָʾ�����ζ����x��(sh��)��̎��UҺ��ϴ�죬�������_�����������BDCEAF��
�ʴ𰸞飺D��C��E��F��
�ڵζ��r(sh��)���۾�Ҫעҕ���F��ƿ?j��)?n��i)��Һ�ɫ��׃�����ȵ���Һ�ɟo(w��)ɫ׃?y��u)�ۼtɫ�����犃�(n��i)�o(w��)�ɫ׃�����f(shu��)������(y��ng)�ζ����K�c(di��n)��
�ʴ𰸞飺�F��ƿ����Һ�ɫ��׃����
�ۈD�픵(sh��)��(j��)������֪3�ε��w�e�`���^����ȥ�����Ę�(bi��o)��(zh��n)ҺV��NaOH��=$\frac{20.05+20.00+19.95}{3}$mL=20.00mL��c��HCl��=$\frac{c��NaOH��V��NaOH��}{V��HCl��}$=$\frac{0.2000mol/L��0.020L}{0.020L}$=0.2000mol/L��
�ʴ𰸞飺0.2000mol/L��
��5��A������(j��)C��HCl��=$\frac{c��NaOH��V��NaOH��}{V��HCl��}$���������Ƙ�(bi��o)��(zh��n)��Һ�Ě������c�л���Na2CO3�s�|(zh��)����ͬ�|(zh��)����NaOH��̼���c�c�}�ᷴ��(y��ng)��̼���c��Ҫ���}�����ښ������c�����Ԛ������c�к���̼���c�r(sh��)�����Ú������c��Һ�w�eƫ��Aƫ�ߣ�
B���ζ��K�c(di��n)�x��(sh��)�r(sh��)����ҕ�ζ��ܵĿ̶ȣ����x��(sh��)ƫ�٣�V��NaOH��ƫ�٣���Bƫ�ͣ�
C��ʢ�bδ֪Һ���F��ƿ�����sˮϴ�^(gu��)��δ�ô��y(c��)Һ��(r��n)ϴ���o(w��)Ӱ푣�
D���ζ����K�c(di��n)�x��(sh��)�r(sh��)�l(f��)�F(xi��n)�ζ��ܼ���̎�Ғ�һ����Һ��V��NaOH��ƫ�ߣ���Dƫ�ߣ�
E��δ�Ø�(bi��o)��(zh��n)Һ��(r��n)ϴ�Aʽ�ζ��ܣ��������c��Ƚ��ͣ���(d��o)�����Ú������c�w�e���࣬��Eƫ�ߣ�
�ʴ𰸞飺ADE��
�c(di��n)�u(p��ng) ���}��������A����(y��ng)����Һ���|(zh��)����ҺpHӋ(j��)�㡢�к͵ζ��Ļ��A(ch��)֪�R(sh��)���}Ŀ�y���еȣ��}���Դ�ע��������늽��|(zh��)��Һ�в�����x��������Ԫ��(qi��ng)�ᡢ�}���һԪ��(qi��ng)�ᣬԇ�}���A(ch��)�ԏ�(qi��ng)����(c��)�،�(du��)�W(xu��)���`���\(y��n)�û��A(ch��)֪�R(sh��)��Q��(sh��)�H��(w��n)�}�����������B(y��ng)��


 ��x��܇(ch��)ϵ�д�
��x��܇(ch��)ϵ�д�
| �꼉(j��) | �����n�� | �꼉(j��) | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
| ���w��ˮ����(y��ng)�Ļ��W(xu��)����ʽ | �Ƿ�����߀ԭ����(y��ng) ����ǡ��� | |
| X+H2O | ||
| Y+H2O | ||
| Z+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}

| A�� | ԓԇ�������|(zh��)������Ȟ�9.2 mol•L-1 | |
| B�� | ԓ����50 mL�c�������~����(y��ng)�ɵõ���(bi��o)��(zh��n)��r��0.46 mol���w | |
| C�� | ����200 mL 4.6mol•L-1��ϡ������ȡԓ����50 mL | |
| D�� | ԓ�����c���w�e��ˮ���������Һ���|(zh��)����?j��n)?sh��)С��49% |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
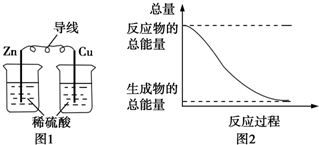
| A�� | �D1��ʾ���b���܌����W(xu��)���D(zhu��n)׃?y��u)���?/td> | |
| B�� | �D2��ʾ�ķ���(y��ng)�����ᷴ��(y��ng) | |
| C�� | �кͷ���(y��ng)�У�����(y��ng)��Ŀ�������������Ŀ������� | |
| D�� | ���W(xu��)����(y��ng)������׃������Ҫԭ���ǻ��W(xu��)�I�Ĕ����c���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
| A�� | Na2O2���w��������ˮ�У�2O${\;}_{2}^{2-}$+2H2O�T4OH-+O2�� | |
| B�� | �������}��Һ��ͨ���^(gu��)����CO2��Ca2++2ClO-+CO2+H2O�TCaCO3��+2HClO | |
| C�� | ̼����}��Һ�е���������NaOH��Һ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| D�� | �����X��Һ�м����^(gu��)����ˮ��Al3++4OH-�TAlO2-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ�����}
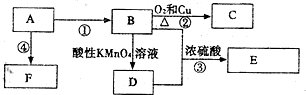
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��(l��i)Դ�� �}�ͣ��x���}
| A�� | C2H6��C9H20һ������ͬϵ�� | |
| B�� | ������ͱ�������Óˮ�s�ϣ���������3�ж��� | |
| C�� | �����������w��(n��i)����������K�D(zhu��n)���������̼��ˮ����ጷ����� | |
| D�� | ���u������Һ�м���ͣ�NH4��2SO4��Һ���г����������ټ�ˮ�����(hu��)�ܽ� |
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)��(c��)�б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��(b��o)ƽ�_(t��i) | �W(w��ng)���к���Ϣ�e��(b��o)���^(q��) | ����p�_�e��(b��o)���^(q��) | ��vʷ̓�o(w��)���x�к���Ϣ�e��(b��o)���^(q��) | �����֙�(qu��n)�e��(b��o)���^(q��)
�`���Ͳ�����Ϣ�e��(b��o)�Ԓ��027-86699610 �e��(b��o)�]�䣺58377363@163.com