
分析 (1)①“原子經濟”是指在化學品合成過程中,所用的所有原材料盡可能多的轉化到最終產物中;
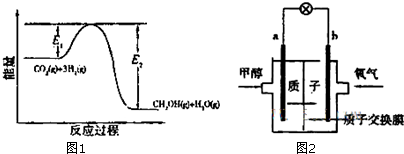
②反應I△H1<0,說明反應是放熱反應,結合能量守恒判斷能量大小;
③根據催化劑的作用分析,催化劑改變反應速率,降低反應的活化能,不改變化學平衡,反應焓變和起始和終了物質能量有關,與變化過程無關;
(3)電解池與電源正極相連的為陽極,與電源負極相連的為電解池的陰極;
(4)根據甲醇燃料電池的原理分析,燃料在負極失電子發生氧化反應,氧氣在正極得到電子發生還原反應,酸性介質中生成水.
解答 解:(1)①“原子經濟”是指在化學品合成過程中,所用的所有原材料盡可能多的轉化到最終產物中,分析反應可知,反應Ⅰ符合“原子經濟”,
故答案為:Ⅰ;
②反應Ⅰ△H1<0,說明反應是放熱反應,則生成物的總能量一定小于反應物的總能量,
故答案為:<;
③在反應體系中加入催化劑,反應速率增大,降低了活化能,E1、E2都減小,反應焓變和起始和終了物質能量有關,與變化過程無關反應熱不變,
故答案為:減小;減小;不變;
(3)甲醇電池中,通入氧氣的b電極為正極,通入甲醇的一極為負極,
故答案為:b;
(4)在酸性介質下,甲醇放電生成CO2,電極方程式為:CH3OH+H2O-6e-=CO2+6H+;
故答案為:CH3OH+H2O-6e-=CO2+6H+.
點評 本題考查了反應熱、化學平衡影響因素、催化劑原理及燃料電池等,難度不大,注意掌握電解池和原電池原理的應用.


 桃李文化快樂暑假武漢出版社系列答案
桃李文化快樂暑假武漢出版社系列答案 優秀生快樂假期每一天全新寒假作業本系列答案
優秀生快樂假期每一天全新寒假作業本系列答案科目:高中化學 來源: 題型:選擇題
| 選項 | 離 子 | 要 求 |
| A | K+、NO3-、Cl-、SO42- | c(K+)<c(Cl-) |
| B | Ca2+、NO3-、CO32-、Cl- | 逐滴加入鹽酸立即有氣體產生 |
| C | Na+、Cu2+、Mg2+、SO42- | 逐滴加入NaOH溶液立即有沉淀產生 |
| D | H+、NH4+、Al3+、SO42- | 逐滴加入NaOH溶液立刻有氣體產生 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子中三個碳原子可能處于同一直線上 | |
| B. | 全氟丙烷的電子式為: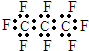 | |
| C. | 相同壓強下,沸點:C3F8<C3H8 | |
| D. | 一個全氟丙烷分子中有10個共用電子對 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
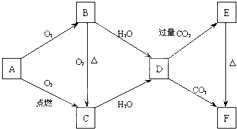 如圖所示,A、B、C、D、E、F為金屬鈉或鈉的化合物.
如圖所示,A、B、C、D、E、F為金屬鈉或鈉的化合物.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 | 雜質 | 試劑 | 主要操作 | |
| A | NaHC03固體 | Na2C03固體 | / | 加熱 |
| B | Al2O3 | Fe2O3 | 鹽酸 | 過濾 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 飽和食鹽水 | 洗氣 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com