

 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr
+HBr| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸點/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
分析 (1)實驗室合成溴苯是苯與液溴在鐵粉作催化劑的條件下發生取代反應生成溴苯和溴化氫;
(2)根據儀器d是吸收揮發出的HBr;
(3)根據該反應為放熱反應及苯、溴的沸點較低容易揮發進行分析;
(4)根據表中數據可知,苯和液溴的沸點較低,容易變成氣體揮發出來;
(5)分離出的粗溴苯中含有未反應的苯,分離互溶的液體,根據沸點不同,利用蒸餾的方法進行分離.
解答 解:(1)在a中加入15mL苯和少量鐵屑,再將b中4.0mL液溴慢慢加入到a中,充分反應生成溴苯和溴化氫,反應的化學方程式為: +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr,
+HBr,
故答案為: +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr;
+HBr;
(2)儀器d中發生的主要反應是吸收HBr氣體,防污染防倒吸,
故答案為:吸收HBr防污染防倒吸;
(3)苯與液溴的反應為放熱反應,若加入液溴速度過快,反應會放出較多的熱量,由于苯和溴的沸點較低,導致苯和溴會揮發出來,影響了溴苯的產率,將b中的液溴慢慢加入到a中,防止反應放出的熱使C6H6、Br2揮發而影響產率,
故答案為:防止反應放出的熱使C6H6、Br2揮發而影響產率;
(4)苯的沸點為80℃,溴的沸點為59℃,二者沸點較低,容易揮發出來,冷凝器冷凝回流的主要物質為:C6H6、Br2,
故答案為:C6H6、Br2;
(5)利用沸點不同,苯的沸點小,被蒸餾出,溴苯留在母液中,所以采取蒸餾的方法分離溴苯與苯,故答案為:蒸餾;
點評 本題考查了苯的性質、制備實驗方案的設計,題目難度中等,涉及了溴苯的制取實驗、物質的分離提純等,清楚制備的原理是解答的關鍵,充分培養了學生的分析、理解能力及靈活應用所學知識解決問題的能力.


 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學 來源: 題型:多選題
| A. | 每生成6.72 L的H2,溶液中AlO2-的數目就增加0.2NA | |
| B. | 每生成0.15 molH2,被還原的水分子數目為0.3NA | |
| C. | 當加入2.7gAl時,轉移的電子數目為0.3NA | |
| D. | 溶液中每增加0.1mol的AlO2-,Na+的數目就增加0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①和④ | B. | ②和③ | C. | ④和⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
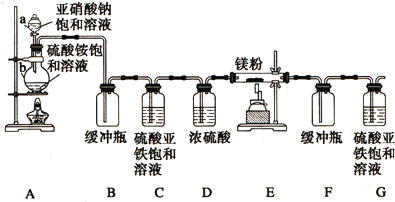
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
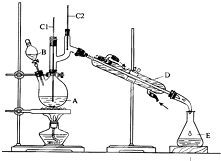 正丁醛是一種化工原料.某實驗小組利用如圖裝置合成正丁醛.
正丁醛是一種化工原料.某實驗小組利用如圖裝置合成正丁醛.| 沸點/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯:
某化學小組采用類似制乙酸乙酯的裝置(如圖),以環己醇制備環己烯:| 密度 (g/cm3) | 熔點 (℃) | 沸點 (℃) | 溶解性 | |
| 環己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 環己烯 | 0.81 | -103 | 83 | 難溶于水 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
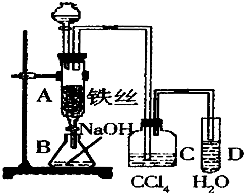 某化學課外小組用如圖裝置制取溴苯.先向分液漏斗中加入苯和液溴,再將混合液慢慢滴入反應器A(A下端活塞關閉)中.
某化學課外小組用如圖裝置制取溴苯.先向分液漏斗中加入苯和液溴,再將混合液慢慢滴入反應器A(A下端活塞關閉)中.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑會使K變化但△H不變 | |
| B. | 使用催化劑會使△H增大,但K不變 | |
| C. | 使用催化劑和提高溫度均可增大H2的轉化率 | |
| D. | 在一密閉容器中,投入濃度均為1mol•L-1的 N2、H2、NH3,平衡前v(正)>v(逆) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com