
| A. | 鎂元素基態原子的核外電子排布式是:1s22s22p63s2 | |
| B. | 鋁元素原子核外共有5種不同運動狀態的電子 | |
| C. | 鈉元素離子半徑比鋁離子半徑大 | |
| D. | 金屬鋁與鈉的最高價氧化物的水化物溶液發生反應的離子方程式為2Al+2OH-+2H2O═2AlO${\;}_{2}^{-}$+3H2↑ |
分析 A.鎂元素原子序數為12,有三個電子層,最外層為2個電子;
B.原子核外有幾個電子就有幾種不同的運動狀態;
C.鈉離子和鋁離子電子層數相同,原子序數越大離子半徑越小;
D.金屬鋁與鈉的最高價氧化物的水化物溶液發生反應生成偏鋁酸鈉和氫氣.
解答 解:A.鎂元素基態原子的核外電子排布式是:1s22s22p63s2 ,故A正確;
B.原子核外有幾個電子就有幾種不同的運動狀態,所以鋁原子核外電子有13種運動狀態,故B錯誤;
C.鈉離子和鋁離子電子層數相同,鈉元素離子半徑比鋁離子半徑大,故C正確;
D.金屬鋁與鈉的最高價氧化物的水化物溶液為氫氧化鈉溶液,鋁和氫氧化鈉溶液發生反應生成偏鋁酸鈉和氫氣,反應的離子方程式2Al+2OH-+2H2O═2AlO2-+3H2↑,故D正確;
故選B.
點評 本題考查了原子結構,主要是原子電子排布、離子半徑大小、物質性質的理解應用,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | HBr、CO2、H2O、CS2 | B. | Cl2、Na2S、HCl、SO2 | ||
| C. | NaCl、HCl、H2O、NaOH | D. | Na2O2、H2O2、H2O、O3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
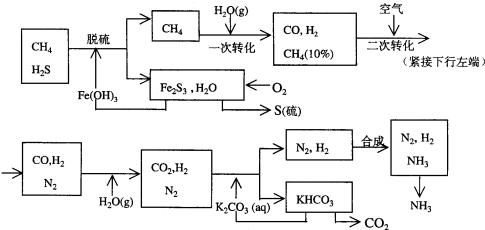
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 30% | B. | 37% | ||
| C. | 50% | D. | 數據不全無法計算 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
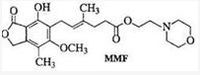
| A. | MMF能發生取代反應和消去反應 | |
| B. | 1 mol MMF能與6 mol 氫氣發生加成反應 | |
| C. | 1 mol MMF能與含3 mol NaOH的水溶液完全反應 | |
| D. | MMF可與Na2CO3溶液反應生成氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 膠體分散質粒子較大,不能透過濾紙 | |
| B. | 液態分散系根據分散質粒子大小分為溶液、膠體和濁液三類 | |
| C. | 利用丁達爾效應可以區分溶液和膠體 | |
| D. | 納米材料分散到液體分散劑中的分散系屬于膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用pH試紙檢測,氨水溶液呈堿性:NH3•H2O=NH4++OH- | |
| B. | 100℃時,測得純水中c(H+)•c(OH-)=3.8×10-13 H2O(l)?H+(aq)+OH-(aq)△H<0 | |
| C. | FeCl3溶液中通入適量SO2,溶液黃色褪去:Fe3++SO2+2H2O=Fe2++SO42-+4H+ | |
| D. | 用CaSO4治理鹽堿地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2通入足量氫氧化鈉溶液中:CO2+2OH-=CO32-+H2O | |
| B. | 用小蘇打治療胃酸過多:HCO${\;}_{3}^{-}$+OH-=CO2↑+H2O | |
| C. | 將Cl2通入水中:Cl2+H2O=Cl-+2H++ClO- | |
| D. | 用FeCl3溶液腐蝕印刷電路板:Fe3++Cu=Fe2++Cu2+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com