
分析 (1)根據元素化合價是否發生變化,以及變化的趨勢判斷物質在氧化還原反應中的表現的性質;
(2)3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合價由0升高為+2價,N元素的化合價由+5價降低為+2價,該反應轉移6e-,以此來解答;
(3)先根據化合價的變化判斷氧化劑和還原劑,然后根據原子守恒配平方程式,再根據電荷守恒判斷n值.
解答 解:(1)2Na+2H2O=2NaOH+H2↑中,H元素化合價降低,被還原,則水只是氧化劑;反應2F2+2H2O=4HF+O2↑中,O元素化合價升高,被氧化,水只是還原劑;反應2H2O$\frac{\underline{\;通電\;}}{\;}$2H2↑+O2↑中,H、O元素化合價變化,水既是氧化劑,又是還原劑,反應CaO+H2O=Ca(OH)2中,H、O元素化合價沒有發生變化,水既不是氧化劑,又不是還原劑,綜上:①水只作氧化劑的是B,故答案為:B;
②水既作氧化劑又作還原劑的是D,故答案為:D;
(2)①該反應中Cu元素化合價由0價變為+2價、部分N元素化合價由+5價變為+2價,其得失電子最小公倍數是6,
用雙線橋標出該反應電子轉移的方向和數目為 ,
,
故答案為: ;
;
②N元素的化合價降低,則HNO3為氧化劑,Cu元素被氧化,則氧化產物為Cu(NO3)2,
故答案為:HNO3;Cu(NO3)2;
③Cu為還原劑,HNO3為氧化劑,3molCu失去電子與2molN得到電子相同,則氧化劑與還原劑的物質的量之比為2:3,故答案為:2:3;
④該反應轉移6e-,若反應中轉移了0.6mol電子,產生的氣體在標準狀況下的體積是0.2mol×22.4L/mol=4.48L,故答案為:4.48L;
(3)該反應中,錳元素的化合價變化為+2價→+7價,失電子化合價升高,錳離子作還原劑;氧元素的化合價不變,所以R元素得電子化合價降低,R2O8n-作氧化劑,即R2O8n-與Mn2+的物質的量之比為5:2,根據各元素的原子守恒寫出并配平該方程式為8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,根據電荷守恒得-5n+2×2=-1×2+(-2×10)+1×16,n=2,故答案為:2.
點評 本題考查氧化還原反應,把握反應中元素的化合價變化為解答的關鍵,側重電子的轉移、氧化劑和還原劑的判斷及計算的考查,注意從化合價角度分析,難度不大.


科目:高中化學 來源: 題型:解答題
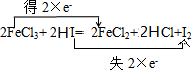 ,當有0.1mol的Fe2+生成時,轉移電子數目為0.1NA.
,當有0.1mol的Fe2+生成時,轉移電子數目為0.1NA.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 需要加熱的反應說明它是吸熱反應 | |
| B. | 氫氣與氧氣反應生成等量的水蒸氣和液態水,前者放出的熱量多 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l),△H=-57.3 kJ/mol,若將含0.5 mol H2SO4的稀硫酸與含1.1 mol NaOH的稀溶液混合,放出的熱量等于 57.3 kJ | |
| D. | 1 mol S完全燃燒放熱297.3 kJ,其熱化學方程式為:S+O2═SO2△H=-297.3 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | z=4 | B. | B 的轉化率是40% | ||
| C. | A 的平衡濃度是1.4 mol•L-1 | D. | 平衡時氣體壓強是原來壓強的0.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 甲醇(CH3OH)和二甲醚(CH3OCH3)被稱為21世紀的新型燃料,具有清潔、高效等優良的性能.
甲醇(CH3OH)和二甲醚(CH3OCH3)被稱為21世紀的新型燃料,具有清潔、高效等優良的性能.| 物質 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 濃度(mol•L-1) | 0.44 | 0.60 | 0.60 |
| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 1molCO、2mol H2 | 1mol CH3OH | 2mol CO、4mol H2 |
| CH3OH的濃度(mol/L) | c1=0.25 | c2 | c3 |
| 反應的能量變化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常數 | K1 | K2 | K3 |
| 反應物轉化率 | α1 | α2 | α3 |
| t2~t3 | t4~t5 | t5~t6 | t7~t8 |
| K4 | K5 | K6 | K7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 陰極 | B. | 陽極 | C. | 正極 | D. | 負極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 某密閉容器中發生如下反應:2X(g)+Y(g)?Z(g);△H<0 如圖表示該反應的速率(v)隨時間(t)變化的關系圖,t2、t3、t5 時刻外界條件有所改變,但都沒有改變各物質的用量.則下列說法中不正確的是( )
某密閉容器中發生如下反應:2X(g)+Y(g)?Z(g);△H<0 如圖表示該反應的速率(v)隨時間(t)變化的關系圖,t2、t3、t5 時刻外界條件有所改變,但都沒有改變各物質的用量.則下列說法中不正確的是( )| A. | t3 時降低了壓強 | |
| B. | t5 時提高了溫度 | |
| C. | t1-t2 時該反應的平衡常數小于 t6時反應的平衡常數 | |
| D. | t6 時刻后反應物的轉化率最低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用蒸發方法使NaCl從溶液中析出時,應邊加熱邊攪拌直至溶液蒸干 | |
| B. | 用10mL量筒量取8.58mL蒸餾水 | |
| C. | 容量瓶定容時觀察液面時俯視,會使配得的溶液濃度偏大 | |
| D. | 用酒精萃取碘水中的I2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com