
【化學選修3:物質結構與性質】Ⅰ.80%左右的非金屬元素在現代技術包括能源、功能材料等領域占有極為重要的地位。
(1)氮及其化合物與人類生產、生活息息相關,基態N原子中電子在2p軌道上的排布遵循的原則是__________,N2F2分子中N原子的雜化方式是_____________,1mol N2F2含有___________個σ鍵.
(2)高溫陶瓷材料Si3N4晶體中鍵角N-Si-N___Si-N-Si(填“>”“<”或“=”),原因是__________;
II.金屬元素在現代工業中也占據極其重要的地位,鈦也被稱為“未來的鋼鐵”,具有質輕,抗腐蝕,硬度大,是宇航、航海、化工設備等的理想材料。
(4)基態鈦原子核外共有________種運動狀態不相同的電子.金屬鈦晶胞如下圖1所示,為_______堆積(填堆積方式).

(5)納米TiO2是一種應用廣泛的催化劑,其催化的一個實例如下圖2.化合物乙的沸點明顯高于化合物甲,主要原因是_____________;化合物乙中采取sp3雜化的原子的電負性由大到小的順序為_____________;
(6)鈣鈦礦晶體的結構如圖3所示.假設把氧離子看做硬球接觸模型,鈣離子和鈦離子填充氧離子的空隙,氧離子形成正八面體,鈦離子位于正八面體中心,則一個鈦離子被________個氧離子包圍。
科目:高中化學 來源:2016屆江蘇省等三校高三第四次模擬化學試卷(解析版) 題型:實驗題
實驗室用下圖所示裝置制備AlC13溶液,并用AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后鍛燒沉淀制備新型的超導材料和發光材料七鋁十二鈣 (12CaO·7Al2O3)。已知A1C13易水解,易升華。
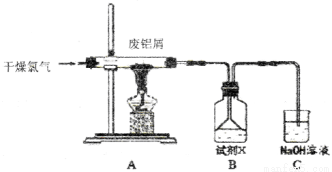
(1)①實驗室用氯酸鉀和濃鹽酸制備氯氣,其離子方程式為____________;
②C裝置的作用____________;
(2)氯氣與廢鋁屑反應生成的AlC13蒸氣溶解在B中,B中盛放的試劑X是____________;為了防止AlC13蒸氣凝華堵塞導管,實驗中可采取的措施是____________(寫出一點)。
(3)B裝置中的AlC13溶液溶解CaCO3時,AlC13溶液和碳酸鈣粉末的混合方式為____________;
(4)實驗要控制碳酸鈣和AlC13的量,要求n(CaCO3): n(A1C13)> 12:14,其原因是____________;
(5)以工業碳酸鈣(含有少量A12O3、Fe2O3雜質)生產二水合氯化鈣(CaC12·2H2O)的方法為:將工業碳酸鈣溶于鹽酸,____________。
已知:幾種離子生成氫氧化物沉淀pH(開始沉淀的pH按金屬離子濃度為1.0mol/L計算)

(實驗中需用到的試劑和儀器有:鹽酸,氫氧化鈣,冰水,pH計)。
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省高三5月模擬三理綜化學試卷(解析版) 題型:選擇題
NA表示阿伏加德羅常數的值,下列有關說法正確的是
A.1L1mol/L的甲醇水溶液中含有氫原子總數為4NA
B.50mL18.4mol/L濃硫酸與足量銅微熱反應,生成SO2分子的數目為0.46NA
C.反應KIO3+6HI=KI+3H2O+3I2中,生成3molI2轉移電子的總數為5NA
D.12g石墨和C60的混合物中質子總數為12NA
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三高考打靶測試理綜化學試卷(解析版) 題型:填空題
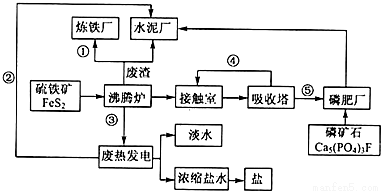
【化學選修2:化學與技術】生態工業園區的建設,不僅僅是體現環保理念更要依據循環經濟理論和充分考慮經濟的可持續發展。下圖是某企業設計的硫酸-磷銨-水泥聯產,海水-淡水多用、鹽-熱-電聯產三大生態產業鏈流程圖。回答下列問題:
(1)從原料、能源、交通角度考慮該企業應建在
A西部山區 B沿海地區 C發達城市 D東北內陸
(2)該流程①、②、③、④、⑤為能量或物質的輸送,請分別寫出輸送的主要物質的化學式或能量形式:①________、②________、③________、④________、⑤________;
(3)沸騰爐發生反應的化學方程式__________;磷肥廠的主要產品是普鈣,其主要成分是___________(填化學式);
(4)熱電廠的冷卻水是________,該流程中濃縮鹽水除提取鹽以外還可提取的物質有_________;(寫出一種即可)
(5)根據現代化工廠沒計理念請提出高爐煉鐵廠廢氣、廢渣及多余熱能的利用設想______________。(寫出兩點即可)
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三高考打靶測試理綜化學試卷(解析版) 題型:選擇題
塑化劑(DCHP)常用于塑料加工,其中一種制備方法如下:
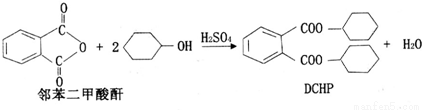
下列說法正確的是( )
A.DCHP的分子式為C20H28O4
B.上述制備DCHP的反應屬于取代反應
C.DCHP苯環上的一氯代物有4種
D.1molDCHP最多可與含4molNaOH的溶液反應
查看答案和解析>>
科目:高中化學 來源:2016屆遼寧省高三全真模擬理綜化學試卷(解析版) 題型:選擇題
一定溫度下,水溶液中H+和OH-的濃度變化如圖所示,下列說法不正確的是( )

A.該溫度下,加入NaHSO4可能引起由b向a的變化
B.該溫度下,pH=2的鹽酸與pH=12的氫氧化鈉溶液等體積混合,所得溶液顯中性
C.該溫度下,加入Na2CO3溶液能引起b向c的變化
D.降低溫度可能引起b向d的變化
查看答案和解析>>
科目:高中化學 來源:2016屆江西省高三考前熱身理綜化學試卷(解析版) 題型:填空題
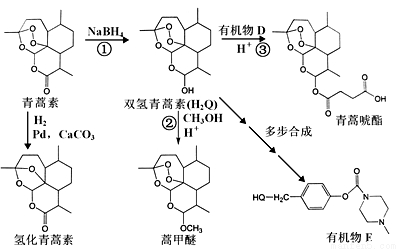
【化學——選修5:有機化學基礎】中國科學家屠呦呦因青蒿素的研究榮獲了2015年諾貝爾化學獎。青蒿素是繼乙氨嘧啶、氯喹、伯喹之后最有效的抗瘧特效藥,具有速效和低毒的特點,曾被世界衛生組織稱做是“世界上唯一有效的瘧疾治療藥物”。由青蒿素合成系列衍生物(它們的名稱和代號如圖所示)的路線如圖:
已知:
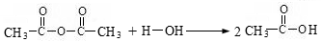
回答下列問題:
(1)青蒿素的分子式為_____________________。
(2)反應①中,有機反應類型為___________;NaBH4的作用是________。(A.氧化劑 B.還原劑 C.催化劑 D.溶劑)
(3)有機物D是分子式為C4H4O3的五元環狀化合物,請寫出D的結構簡式 。
(4)青蒿唬酯能夠發生的反應類型有 。
A.酯化反應 B.水解反應 C.還原反應 D.加聚反應
(5)以H2Q表示雙氫青蒿素,寫出反應②(雙氫青蒿素和甲醇反應)的化學方程式_________。
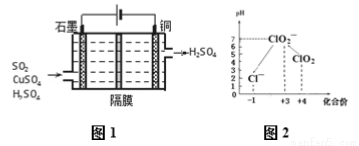
(6)從雙氫青蒿素(H2Q)出發,可通過多步反應合成出有機物E。合成過程中,有機原料除H2Q、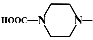 外,還需含苯環的二羥基化合物F,寫出有機物F與NaOH溶液反應的離子反應方程式___________________________,有機物G是F的同分異構體,有機物G遇FeCl3溶液顯紫色,且有4種不同類型的氫,其個數比為3:2:2:1,則符合條件的有機物G的同分異構體有_____種。寫出其中一種的結構簡式 。
外,還需含苯環的二羥基化合物F,寫出有機物F與NaOH溶液反應的離子反應方程式___________________________,有機物G是F的同分異構體,有機物G遇FeCl3溶液顯紫色,且有4種不同類型的氫,其個數比為3:2:2:1,則符合條件的有機物G的同分異構體有_____種。寫出其中一種的結構簡式 。
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三考前模擬理綜化學試卷(解析版) 題型:填空題
氮、硫、氯及其化合物是中學化學重要的組成部分.
(1)氨氣燃料電池使用的電解質溶液是 KOH 溶液,電池反應為:4NH3 +3O2 =2N2 +6H2O.該電池負極的電極反應式為___________;用該電池進行粗銅(含 Al、Zn、Ag、Pt、Au 等雜質)的電解精煉,以CuSO4溶液為電解質溶液,下列說法正確的是__________。
a.電能全部轉化為化學能
b.SO42﹣的物質的量濃度不變(不考慮溶液體積變化)
c.溶液中Cu2+向陽極移動
d.利用陽極泥可回收Ag、Pt、Au等金屬
e.若陽極質量減少64g,則轉移電子數為2NA個
(2)已知KSP(BaSO 4)=1.0×10﹣10 ,KSP(BaCO3)=2.5×10﹣9 。
某同學設想用下列流程: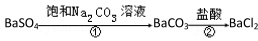 ,得到 BaCl2,則①的離子方程式為__________________,該反應的平衡常數K=__________;
,得到 BaCl2,則①的離子方程式為__________________,該反應的平衡常數K=__________;
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省高二6月月考化學試卷(解析版) 題型:填空題
用KMnO4氧化溶質質量分數為36.5%的鹽酸。反應方程式如下:
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(1)若此鹽酸的密度為1.2g/cm3,其物質的量濃度為_________________________;
(2)用雙線橋表示電子的得失_________________________;
(3)此反應中氧化劑是_________,氧化產物____________;
(4)若有xmolKMnO4參加反應,則轉移電子的物質的量為____________;
(5)15.8gKMnO4完全反應,產生標準狀況下Cl2的體積為_________,同時有________molHCl被氧化。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com