
| 化學式 | CH3COOH | H2CO3 | HClO | |
| 電離平衡 常數 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
分析 (1)酸根離子對應酸的酸性越強,該離子的水解程度越小,溶液的pH越小;
(2)0.1mol/L的CH3COOH溶液加水稀釋過程中,氫離子與醋酸根離子物質的量增大,醋酸分子物質的量減小,濃度減小,酸性減弱,水的離子積常數不變,醋酸的電離平衡常數不變;
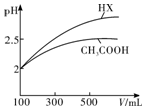
(3)據圖分析,加水稀釋的過程中,HX的pH變化比較快,說明HX的酸性比醋酸強;
(4)標準狀況下,將1.12L CO2通入100mL 1mol•L-1的NaOH溶液中,1.12L CO2的物質的量為:$\frac{1.12L}{22.4L/mol}$=0.05mol,氫氧化鈉的物質的量為:1mol•L-1×0.1L=0.1mol,二者恰好完全反應生成碳酸鈉,溶液中存在電荷守恒和物料守恒;
(5)CH3COOH與CH3COONa的混合溶液中,存在電荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),根據溶液中的電荷守恒和物料守恒來計算.
解答 解:(1)四種溶液的溶質都是強堿弱酸鹽,水解程度大小為:CO32->ClO->HCO3->CH3COO-,水解均顯堿性,水解程度越大,堿性越強,所以堿性順序是:Na2CO3>NaClO>NaHCO3>CH3COONa,
即pH由小到大的排列順序為:CH3COONa<NaHCO3<NaClO<Na2CO3,即:a<d<c<b,
故答案為:a<d<c<b;
(2)0.1mol/L的CH3COOH溶液加水稀釋過程中,氫離子與醋酸根離子物質的量增大,濃度減小,酸性減弱,
A、氫離子濃度減小,故A錯誤;
B、加水稀釋過程中,氫離子物質的量增大,醋酸分子物質的量減小,所以$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大,故B正確;
C、水的離子積常數不變,故C錯誤;
D、醋酸溶液加水稀釋時酸性減弱,氫離子濃度減小氫氧根離子濃度增大,所以$\frac{c(O{H}^{-})}{c({H}^{+})}$增大,故D正確;
E、醋酸的電離平衡常數不變,故E錯誤;
故答案為:BD;
(3)據圖分析,加水稀釋的過程中,HX的pH變化比較快,說明HX的酸性比醋酸強,HX的電離平衡常數比醋酸大,
故答案為:大于;
(4)標準狀況下,將1.12L CO2通入100mL 1mol•L-1的NaOH溶液中,1.12L CO2的物質的量為:$\frac{1.12L}{22.4L/mol}$=0.05mol,氫氧化鈉的物質的量為:1mol•L-1×0.1L=0.1mol,二者恰好完全反應生成碳酸鈉,
①溶液中存在質子守恒:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),
故答案為:c(H+)+c(HCO3-);
②碳酸鈉溶液中存在電荷守恒:c(H+)+c(Na+)=2c(CO32-)+c(HCO3-)+c(OH-),
故答案為:2c(CO32-)+c(HCO3-)+c(OH-);
(5)CH3COOH與CH3COONa的混合溶液中,存在電荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),所以c(CH3COO-)-c(Na+)=c(H+)-c(OH-)=10-6mol/L-10-8mol/L=9.9×10-7mol/L,
故答案為:9.9×10-7.
點評 本題考查了鹽的水解、弱電解質的電離及其影響、電離平衡常數的應用等,題目難度中等,試題知識點較多、綜合性較強,充分考查了學生的分析、理解能力及靈活應用所學知識的能力.


 課時訓練江蘇人民出版社系列答案
課時訓練江蘇人民出版社系列答案 黃岡經典趣味課堂系列答案
黃岡經典趣味課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 開啟啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 將盛有二氧化氮和四氧化二氮混合氣的密閉容器置于冷水中,混合氣體顏色變淺- | |
| C. | 向氯水中加CaCO3后,溶液漂白性增強 | |
| D. | 500℃左右比室溫更有利于合成NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | NH3•H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鍍銅鐵制品鍍層破損后,鐵制品比破損前更容易生銹 | |
| B. | 標準狀況下,22.4 L Cl2與足量NaOH溶液反應,轉移電子數為2mol | |
| C. | 水的離子積常數Kw隨著溫度的升高而增大,說明水的電離是放熱反應 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固體,CO32-水解程度減小,溶液的pH減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入過量氨水,有白色沉淀生成,則原溶液一定有Al3+ | |
| B. | FeCl3、CuCl2的混合溶液中加入鐵粉,充分反應后仍有固體剩余,加入KCSN溶液可能變成血紅色 | |
| C. | 鋅與濃硫酸不反應,與稀硫酸反應生成氫氣 | |
| D. | 加入NaOH溶液,加熱后產生的氣體能使濕潤的紅色石蕊試紙變藍,則原溶液一定有NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N、M均不能發生銀鏡反應 | B. | M中可能沒有甲基 | ||
| C. | N可發生消去反應 | D. | N分子中含有甲基 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com