
| A. | a點所得溶液中:2c(H2SO3)+c(SO32-)=0.1 mol•L-1 | |
| B. | b點所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | |
| C. | c點所得溶液中:c(Na+)<3c($HS{{{O}_{3}}^{-}}_{\;}$) | |
| D. | d點所得溶液中:c(Na+)>c(SO32-)>c(HSO3-) |
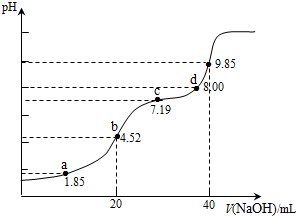
分析 A.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液,a點溶液中溶質為H2SO3和NaHSO3,PH=1.85=Pa1,則c(H2SO3)=c(HSO3-)依據物料守恒判斷;
B.b點是用0.1mol•L-1NaOH溶液20ml滴定20mL0.1mol•L-1H2SO3溶液,恰好反應生成NaHSO3,溶液顯酸性,依據溶液中電荷守恒和物料守恒計算分析判斷;
C.c點PH=7.19=PKa2,依據平衡常數溶液顯堿性,溶液中溶質主要為Na2SO3,SO32-+H2O?HSO3-+OH-,Kh=$\frac{c(O{H}^{-})c(HS{{O}_{3}}^{-})}{c(S{{O}_{3}}^{2-})}$=$\frac{Kw}{K{a}_{2}}$,c(OH-)=$\frac{Kw}{c({H}^{+})}$,c(HSO3-)=c(SO32-),結合溶液中物料守恒分析;
D.加入氫氧化鈉溶液40ml,NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液恰好反應生成Na2SO3,d點溶液中主要是Na2SO3和少量NaHSO3.
解答 解:A.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液,a點溶液中溶質為H2SO3和NaHSO3,PH=1.85=Pa1,電離平衡常數表達式得到則c(H2SO3)=c(HSO3-),溶液體積大于20ml,a點所得溶液中:c(H2SO3)+c(SO32-)+c(HSO3-)=2c(H2SO3)+c(SO32-)<0.1 mol•L-1 ,故A錯誤;
B.b點是用0.1mol•L-1NaOH溶液20ml滴定20mL0.1mol•L-1H2SO3溶液,恰好反應生成NaHSO3,溶液顯酸性,溶液中電荷守恒c(Na+)+c(H+)=c(HSO3-)+c(OH-)+2c(SO32-),物料守恒c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3),得到:c(H2SO3)+c(H+)=c(SO32-)+c(OH-),故B正確;
C.c點PH=7.19=PKa2,依據平衡常數溶液顯堿性,溶液中溶質主要為Na2SO3,SO32-+H2O?HSO3-+OH-,Kh=$\frac{c(O{H}^{-})c(HS{{O}_{3}}^{-})}{c(S{{O}_{3}}^{2-})}$=$\frac{Kw}{K{a}_{2}}$,c(OH-)=$\frac{Kw}{c({H}^{+})}$,帶入計算得到:c(HSO3-)=c(SO32-),溶液中2n(Na)=3c(S),2c(Na+)=3[c(SO32-)+c(H2SO3)+c(HSO3-)]=3[c(H2SO3)+2c(HSO3-)],c(Na+)>3c($HS{{{O}_{3}}^{-}}_{\;}$),故C錯誤;
D.加入氫氧化鈉溶液40ml,NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液恰好反應生成Na2SO3,d點溶液中主要是Na2SO3和少量NaHSO3,溶液中離子濃度c(Na+)>c(SO32-)>c(HSO3-),故D正確;
故選BD.
點評 本題考查了圖象變化的分析,酸堿反應溶液酸堿性,鹽類水解原理,電解質溶液中離子濃度大小的比較方法等知識,題目難度較大.


 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:高中化學 來源: 題型:選擇題
| A. | 濃度均為0.01 mol•L-1的醋酸和硫酸溶液中分別加入足量鋅片,生成H2的起始速率相等 | |
| B. | 0.1 mol•L-1的NaHCO3溶液中:[Na+]=[HCO3-]+[CO32-]+[H2CO3] | |
| C. | pH=11的氨水與pH=3的鹽酸等體積混合:[Cl-]=[NH4+]>[OH-]=[H+] | |
| D. | 將0.1 mol的CH3COOH和0.1 mol的CH3COONa溶于水中,配成1L混合溶液.測得溶液的pH<7,則混合液中[CH3COO-]<[Na+] |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
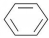 +HNO3(濃)$\frac{\underline{\;\;\;濃硫酸\;\;\;}}{50~60℃}$
+HNO3(濃)$\frac{\underline{\;\;\;濃硫酸\;\;\;}}{50~60℃}$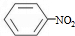 +H2O設計一個實驗制取一定量的純凈硝基苯.有關信息見下表:
+H2O設計一個實驗制取一定量的純凈硝基苯.有關信息見下表:| 物質 | 熔點/℃ | 沸點/℃ | 相對密度/(20℃) | 毒性 | 水溶性 |
| 苯 | 5.5 | 80.1 | 0.8794 | 有 | 不溶于水 |
| 硝酸 | -41.59 | 83 | 1.503 | - | 易溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 有 | 不溶于水 |
| 硫酸 | 10.0 | 338 | 1.84 | - | 易溶于水 |

| 1 | 用蒸餾水洗滌反應混合液,分液后取下層液體 |
| 2 | |
| 3 | |
| 4 | |
| 5 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1個 | B. | 2個 | C. | 3個 | D. | 4個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol SiO2晶體中,含有2NA個Si-O共價鍵 | |
| B. | 常溫下,4.4 g CO2和N2O混合物中所含有的原子數為0.3NA | |
| C. | 0.2 mol Cl2溶解于等體積的水中,轉移電子數為0.2NA | |
| D. | 標準狀況下,11.2L 四氯化碳所含分子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | Y | ||
| Z | W | Q |
| A. | 由Y與W形成的氧化物溶于水一定是強酸 | |
| B. | Z和Y組成的物質是原子晶體 | |
| C. | Z與Q形成的物質能與H2在一定條件下反應 | |
| D. | X和Y均存在同素異形體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 40mL | B. | 72mL | C. | 80mL | D. | 128mL |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com