
分析 ①中和滴定有檢漏、洗滌、潤洗、裝液、取待測液于錐形瓶,然后加入指示劑進行滴定等操作;
②如溶液顏色變化且半分鐘內不變色,可說明達到滴定終點;
③滴定管0刻度在上,滴定前應調節到零刻度或零稍下的某一刻度,為減小誤差,尖嘴部分應充滿液體,無氣泡;
④根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析不當操作對V(標準)的影響,以此判斷濃度的誤差.
解答 解:①操作的步驟是選擇滴定管檢漏(C),然后洗滌(E)、裝液(D)、使尖嘴充滿溶液、固定在滴定臺上,然后調節液面記下讀數.用待測的NaOH溶液潤洗堿式滴定管(B).再取待測液于錐形瓶(A),然后加入指示劑進行滴定(G),另取錐形瓶,再重復滴定操作一次(F),所以順序為:C→E→D→B→A→G→F,
故答案為:C;D;A;G;F;
②本實驗是用鹽酸滴定NaOH溶液,用酚酞作指示劑,所以終點時,現象是當滴加最后一滴鹽酸時,溶液由紅色變為無色,且半分鐘內不褪色,
故答案為:當滴加最后一滴鹽酸時,溶液由紅色變為無色,且半分鐘內不褪色;
③滴定管0刻度在上,滴定前應調節到零刻度或零稍下的某一刻度,為減小誤差,尖嘴部分應充滿液體,無氣泡,
故答案為:0或0刻度一下某一刻度;充滿液體;
④酸式滴定管未用標準鹽酸潤洗就直接注入標準鹽酸,鹽酸被稀釋,濃度降低,造成V(標準)偏大,根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析可知c(待測)偏高,
堿式滴定管未用待測的NaOH溶液潤洗,待測NaOH溶液被稀釋,造成V(待測)偏大,根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$分析可知c(待測)偏低,
故答案為:偏高;偏低.
點評 本題綜合考查酸堿中和滴定,側重于化學實驗基本操作以及物質的含量的測定等問題,題目難度不大,在學習中注意把握相關基本實驗方法,注意根據c(待測)=$\frac{c(標準)×V(標準)}{V(待測)}$進行誤差分析.


科目:高中化學 來源: 題型:選擇題
| A. | “殲-20”飛機上使用的碳纖維是一種新型的有機高分子材料 | |
| B. | 用活性炭為糖漿脫色和用臭氧漂白紙漿,原理相似 | |
| C. | 燃料電池的燃料都在負極發生氧化反應 | |
| D. | Fe3O4俗稱鐵紅,常做紅色油漆和涂料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | ① | ② | ③ | 實驗結論 | 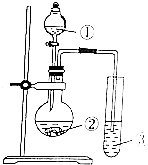 |
| A | 濃醋酸 | 石灰石 | Na2SiO3溶液 | 酸性:醋酸>碳酸>硅酸 | |
| B | 濃鹽酸 | KMnO4 | KBr溶液 | 氧化性:KMnO4>Cl2>Br2 | |
| C | 稀硫酸 | FeS | SO2水溶液 | BaS可還原SO2 | |
| D | 鹽濃酸 | 濃硫酸 | BaSO3懸濁液 | BaSO3可溶于鹽酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖為兩套實驗裝置.
如圖為兩套實驗裝置.
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
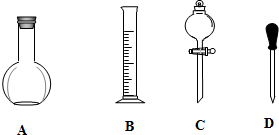 實驗室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題.
實驗室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
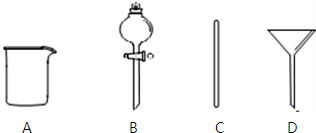 實驗室需要0.1mol•L-1NaOH溶液480mL.
實驗室需要0.1mol•L-1NaOH溶液480mL.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 反應中氧化劑和還原劑的質量比為1:2 | |
| B. | 反應中生成了8g Cu2S | |
| C. | 反應中有0.2×6.02×1023個電子轉移 | |
| D. | 反應中有1.6g硫被氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com