
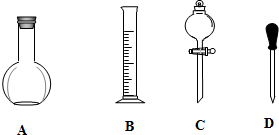
 實驗室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題.
實驗室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題.分析 (1)依據配制一定物質的量濃度溶液的一般步驟選擇需要儀器,確定用不到的儀器和缺少的儀器;
(2)依據容量瓶構造及使用方法及注意事項解答;
(3)依據配制溶液體積選擇合適的容量瓶,依據m=CVM計算需要溶質的質量;
(4)依據C=$\frac{1000ρω}{M}$計算濃硫酸的物質的量濃度,依據溶液稀釋規律計算需要濃硫酸體積,依據量取濃硫酸體積選擇合適的量筒;
(5)根據c=$\frac{n}{V}$并結合溶質的物質的量n和溶液的體積V的變化來進行誤差分析.
解答 解:(1)配制一定物質的量濃度溶液的一般步驟:計算、稱量或者量取、溶解或者稀釋、移液、洗滌、定容、搖勻,用到的儀器:托盤天平、藥匙、量筒、燒杯、玻璃棒、500mL容量瓶(450mL沒有此規格的容量瓶)、膠頭滴管,用不到平底燒瓶和分液漏斗,還缺少的儀器:燒杯、玻璃棒、500mL容量瓶;
故答案為:AC;燒杯、玻璃棒、500mL容量瓶;
(2)A.容量瓶帶有瓶塞,使用前應檢查是否漏水,故A正確;
B.容量瓶用水洗凈后,再用待配溶液洗滌,導致溶質的物質的量偏大,溶液濃度偏高,故B錯誤;
C.容量瓶為精密儀器,不能用來溶解固體,故C錯誤;
D.容量瓶為精密儀器,不能用來稀釋濃溶液,故D錯誤;
E.定容后,蓋好瓶塞,用食指頂住瓶塞,另一只手托住瓶底,把容量瓶反復倒轉多次,搖勻,故E正確;
故選:BCD;
(3)需要0.1mol/LNaOH溶液450mL,應選擇500mL容量瓶,實際配制500mL溶液,需要溶質的質量m=0.1mol/L×40g/mol×0.5L=2.0g,
故答案為:2.0;
(4)質量分數為98%、密度為1.84g/cm3的濃硫酸的物質的量濃度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,設需要濃硫酸體積為V,則依據溶液稀釋前后所含溶質的物質的物質的量濃度不變得18.4mol/L×V=0.5L×0.5mol/L,解得V=0.0136L,即13.6mL;需要用15mL量筒量取,
故答案為:13.6; 15;
(5)①液體具有熱脹冷縮的性質,濃硫酸溶解后未冷至室溫即進行定容,冷卻至室溫時體積變小,溶質不變,溶液濃度偏高,
故答案為:偏高;
②定容時俯視刻度線,導致溶液體積偏小,所以溶液濃度偏高,
故答案為:偏高.
點評 本題考查了配制一定物質的量濃度的溶液的方法,明確配制原理和步驟是解題關鍵,注意容量瓶、量筒規格的選取方法,題目難度不大.


 全能練考卷系列答案
全能練考卷系列答案 一課一練課時達標系列答案
一課一練課時達標系列答案科目:高中化學 來源: 題型:選擇題
| A. | 乙醇可以氧化為乙醛或乙酸,三者都能發生酯化反應 | |
| B. | 苯酚鈉溶液中通入CO2生成苯酚,表明苯酚的酸性比碳酸的強 | |
| C. | 乙酸乙酯在酸性或堿性條件下都能發生水解反應 | |
| D. | 可用FeCl3溶液來區分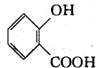 和 和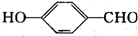 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.8g的SCN-中所含電子數為3NA | |
| B. | 0.1mol的CH3CH${\;}_{{2}^{\;}}$18O2H中所含中子數2.3NA | |
| C. | 10gCaCO3和KHCO3的混合物中所含質子數為5NA | |
| D. | 7.9gNH4HCO3固體中所含分子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SiO2是難溶于水的酸性氧化物 | |
| B. | 高溫下SiO2與碳酸鹽反應生成CO2 | |
| C. | SiO2不能與任何酸反應 | |
| D. | 碳化硅(SiC)具有金剛石的結構,硬度很大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
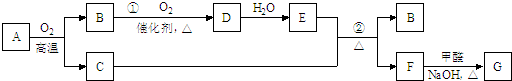
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com