
【題目】NH4Al(SO4)2是食品加工中最為快捷的食品添加劑,用于焙烤食品中;NH4HSO4在分析試劑、醫藥、電子工業中用途廣泛。請回答下列問題:
(1)相同條件下,0.1mol/L NH4Al(SO4)2中c(NH4+) ______ ![]() 填“等于”、“大于”或“小于”0.1mol/LNH4HSO4中c(NH4+)。
填“等于”、“大于”或“小于”0.1mol/LNH4HSO4中c(NH4+)。
(2)如圖是0.1mol/L電解質溶液的pH隨溫度變化的圖象:
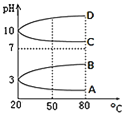
①其中符合0.1mol/L NH4Al(SO4)2的pH隨溫度變化的曲線是 ______ (填寫字母);
②20℃時,0.1mol/L NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______mol/L
(3)室溫時,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到的溶液pH與NaOH溶液體積的關系曲線如圖所示。試分析圖中a、b、c、d四個點,水的電離程度最大的是 ______ ;在b點,溶液中各離子濃度由大到小的排列順序是 ______
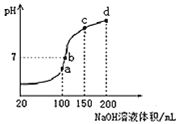
(4)已知Al(OH)3為難溶物(常溫下,Ksp[Al(OH)3]=2.0×10-33)當溶液pH=5時,某溶液中的Al3+ ______ ![]() 填“能”或“不能”
填“能”或“不能”![]() 完全沉淀(溶液中的離子濃度小于1×10-5mol/L時,沉淀完全)
完全沉淀(溶液中的離子濃度小于1×10-5mol/L時,沉淀完全)
【答案】小于 A 10-3 a c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) 能
【解析】
(1)相同條件下,鋁離子抑制銨根離子水解程度小于氫離子,銨根離子水解程度越大,溶液中銨根離子濃度越小;
(2)①NH4Al(SO4)2中銨根離子和鋁離子水解導致溶液呈酸性,則pH<7,升高溫度促進水解,溶液酸性增強;
②任何電解質溶液中都存在電荷守恒,根據電荷守恒計算;
(3)a、b、c、d四個點,根據反應量的關系,a點恰好消耗完H+,溶液中只有(NH4)2SO4與Na2SO4;b、c、d三點溶液均含有NH3H2O,(NH4)2SO4可以促進水的電離,而NH3H2O抑制水的電離.b點溶液呈中性;
(4)根據濃度積與溶度積常數相對大小判斷,如果濃度積大于溶度積常數,則有沉淀生成,否則沒有沉淀生成.
(1)相同條件下,鋁離子抑制銨根離子水解程度小于氫離子,銨根離子水解程度越大,溶液中銨根離子濃度越小,所以NH4Al(SO4)2中銨根離子水解程度大于NH4HSO4,則NH4Al(SO4)2中c(NH4+)小于0.1mol/LNH4HSO4中c(NH4+);
(2)①NH4Al(SO4)2中銨根離子和鋁離子水解導致溶液呈酸性,則pH<7,升高溫度促進水解,溶液酸性增強,溶液的pH減小,故選A;
②根據電荷守恒得2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3mol/L [c(OH-)太小,可忽略];
(3)a、b、c、d四個點,根據反應量的關系,a點恰好消耗完H+,溶液中只有(NH4)2SO4與Na2SO4;b、c、d三點溶液均含有NH3H2O,(NH4)2SO4可以促進水的電離,而NH3H2O抑制水的電離,b點溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3H2O三種成分,a點時c(Na+)=c(SO42-),b點時c(Na+)>c(SO42-),根據N元素與S元素的關系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);
(4)pH=5的溶液中c(OH-)=10-9mol/L,c(Al3+)=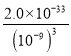 mol/L=2.0×10-6mol/L<1×10-5 mol/L,所以能完全沉淀。
mol/L=2.0×10-6mol/L<1×10-5 mol/L,所以能完全沉淀。


科目:高中化學 來源: 題型:
【題目】![]() 時,一定量的
時,一定量的![]() 與鹽酸混合所得溶液中,部分含碳微粒的物質的量分數
與鹽酸混合所得溶液中,部分含碳微粒的物質的量分數![]() 與pH的關系如圖所示。下列說法正確的是
與pH的關系如圖所示。下列說法正確的是
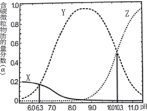
A.曲線X表示的微粒為![]()
B.![]() 時,
時,![]()
C.![]() 時,
時,![]()
D.![]() 時,
時,![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“位置”、“結構”和“性質”是我們學習元素周期律的重要思路。
(1)我們可以根據原子結構示意圖來推測元素在周期表中的位置,以下為X元素的原子結構示意圖(未畫全):
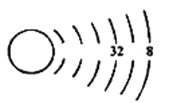
請寫出X元素在周期表中的位置_____________________。
(2)我們也可以根據物質性質推測該元素在元素周期表中的位置,如Y元素最高價氧化物既可以溶于濃鹽酸,也可以溶于NaOH溶液;其最高價氧化物對應的水化物既可以與酸反應,也可以與堿反應;1mol該元素最高價氧化物對應的水化物在與鹽酸反應時,最多能消耗4molHCl。請寫出Y元素在周期表中的位置_____________________。
(3)反過來,知道了元素的位置關系,我們可以推測元素性質或者元素對應的單質及化合物的性質。四種短周期元素在周期表中的位置如下圖所示,其中只有M為金屬元素。則Y和Z原子半徑更大的是____(填元素符號或化學式,下同),Y和X最高價氧化物對應水化物的酸性更弱的是______。
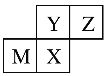
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物W用作調香劑、高分子材料合成的中間體等,制備W的一種合成路線如圖。
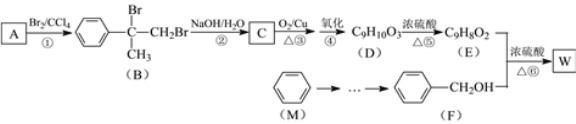
已知:![]() +CH3Cl
+CH3Cl![]()
![]() +HCl
+HCl
請回答下列問題:
(1)A的化學式是___,F的化學名稱是___。
(2)②和⑤的反應類型分別____、____。
(3)E中含氧官能團是___(寫名稱),D聚合生成高分子化合物的結構簡式為___。
(4)寫出反應⑥的化學方程式:___。
(5)反應③的化學方程式:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新型儲氫材料是開發利用氫能的重要研究方向.
(1)Ti(BH4)3是一種儲氫材料,可由TiCl4和LiBH4反應制得.
①基態Cl原子中,電子占據的最高能層符號為_____,該能層具有的原子軌道數為_____.
②LiBH4由Li+和BH4﹣構成,BH4﹣的立體結構是_____,B原子的雜化軌道類型是_____.
Li、B、H元素的電負性由大到小排列順序為_____.
(2)金屬氫化物是具有良好發展前景的儲氫材料.
①LiH中,離子半徑Li+_____H﹣(填“>”、“=”或“<”).②某儲氫材料是第三周期金屬元素M的氫化物.M的部分電離能如表所示:
I1/kJmol﹣1 | I2/kJmol﹣1 | I3/kJmol﹣1 | I4/kJmol﹣1 | I5/kJmol﹣1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是_____(填元素符號).
(3)NaH具有NaCl型晶體結構,已知NaH晶體的晶胞參數a=488pm(棱長),Na+半徑為102pm,H﹣的半徑為_____,NaH的理論密度是___________gcm﹣3(只列算式,不必計算出數值,阿伏加德羅常數為NA)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋰錳電池的體積小、性能優良,是常用的一次電池。該電池反應原理如圖所示,其中電解質LiClO4,溶于混合有機溶劑中,Li+通過電解質遷移入MnO2晶格中,生成LiMnO2。 回答下列問題:

(1)外電路的電流方向是由________極流向________極(填字母)。
(2)電池正極反應式為___________________________________。
(3)是否可用水代替電池中的混合有機溶劑?________(填“是”或“否”),原因是________________________________________________________________。
(4)MnO2可與KOH和KClO3在高溫下反應,生成K2MnO4,反應的化學方程式為_______________________________________________。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物質的量之比為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃和101kPa時,乙烷、乙炔和丙烯組成的混合烴24mL,與過量氧氣混合并完全燃燒,通過濃硫酸后,恢復到原來的溫度和壓強,氣體總體積縮小了54mL,原混合烴中乙炔的體積分數為( )
A.75%B.50%C.25%D.20%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金剛烷胺(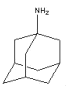 )是最早用于抑制流感病毒的抗病毒藥,每片感康(復方氨酚烷胺片)含鹽酸金剛烷胺100mg。金剛烷胺一般是由金剛烷合成的。金剛烷是一種重要的化工原料,由環戊二烯合成金剛烷的路線如下:
)是最早用于抑制流感病毒的抗病毒藥,每片感康(復方氨酚烷胺片)含鹽酸金剛烷胺100mg。金剛烷胺一般是由金剛烷合成的。金剛烷是一種重要的化工原料,由環戊二烯合成金剛烷的路線如下:
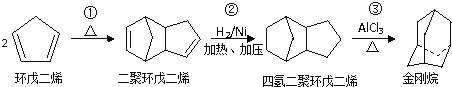
請回答下列問題:
(1)金剛烷的碳架結構相當于是金剛石晶格網絡中的一個晶胞,故得金剛烷這個名字。它可看作是由四個等同的六元環組成的空間構型。金剛烷的二氯代物有___種。上述合成金剛烷的路線中,反應①的反應類型為___。
(2)金剛烷與四氫二聚環戊二烯的關系是___。(填字母)
a.均為環烴 b.均為烷烴 c.互為同系物 d.互為同分異構體
(3)下面是以環戊烷為原料制備環戊二烯的合成路線:
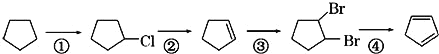
反應④的化學方程式為____。
(4)在有機分析中,常用臭氧氧化分解來確定有機物中碳碳雙鍵的位置與數目。
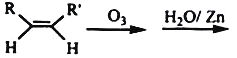 RCHO+R’CHO
RCHO+R’CHO
A是金剛烷的一種同分異構體,經臭氧氧化后的產物僅為一種,其結構為![]() ,試寫出A可能的結構簡式(任寫一種)___。
,試寫出A可能的結構簡式(任寫一種)___。
(5)B是二聚環戊二烯的同分異構體,B分子結構中有一個甲基,B能使溴的四氯化碳溶液褪色,B經高錳酸鉀酸性溶液加熱氧化可以得到對苯二甲酸(提示:苯環上的烷基(—CH3、—CH2R、—CHR2)或烯基側鏈經高錳酸鉀酸性溶液氧化得羧基),B的結構有多種,其中核磁共振氫譜為6組峰,且面積比為3﹕2﹕2﹕2﹕1﹕2的結構簡式是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學實驗小組欲測定鐵的氧化物![]() 樣品組成,查閱資料發現:甲酸
樣品組成,查閱資料發現:甲酸![]() 是一種有刺激性氣味的無色液體,易揮發,有較強的還原性,熔點
是一種有刺激性氣味的無色液體,易揮發,有較強的還原性,熔點![]() ,沸點
,沸點![]() ,能與水、乙醇互溶,甲酸與濃硫酸共熱可制備一氧化碳:HCOOH
,能與水、乙醇互溶,甲酸與濃硫酸共熱可制備一氧化碳:HCOOH![]() H2O+CO↑,制備時先加熱濃硫酸至
H2O+CO↑,制備時先加熱濃硫酸至![]() ,再逐滴滴入甲酸。根據以上信息設計了實驗裝置,如圖所示:
,再逐滴滴入甲酸。根據以上信息設計了實驗裝置,如圖所示:
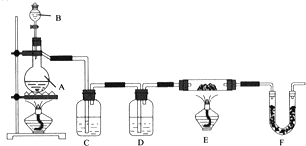
請回答下列問題:
![]() 儀器中裝入的試劑:B ______ 、C ______ 、D ______。
儀器中裝入的試劑:B ______ 、C ______ 、D ______。
![]() 該實驗裝置A儀器中須添加一種玻璃儀器,其名稱為______;連接好裝置后應首先______。
該實驗裝置A儀器中須添加一種玻璃儀器,其名稱為______;連接好裝置后應首先______。
![]() “加熱反應管E”和“從B向A逐滴滴加液體”這兩步操作應該先進行的是______
“加熱反應管E”和“從B向A逐滴滴加液體”這兩步操作應該先進行的是______![]() 在這兩步之間還應進行的操作是______。
在這兩步之間還應進行的操作是______。
![]() 反應過程中F管
反應過程中F管![]() 內盛堿石灰
內盛堿石灰![]() 逸出的氣體是______,其處理方法是______。
逸出的氣體是______,其處理方法是______。
![]() 測得下列數據
測得下列數據![]() 空E管的質量為
空E管的質量為![]() ;
;![]() 管和
管和![]() 樣品的總質量為
樣品的總質量為![]() ;
;![]() 反應后冷卻至室溫稱量E管和鐵粉的總質量為
反應后冷卻至室溫稱量E管和鐵粉的總質量為![]() 經確認樣品全部變為鐵粉
經確認樣品全部變為鐵粉![]() 計算可知該鐵的氧化物化學式為______。
計算可知該鐵的氧化物化學式為______。
![]() 設計實驗證明:
設計實驗證明:
![]() 甲酸的酸性比碳酸的強______。
甲酸的酸性比碳酸的強______。
![]() 的氧化性比
的氧化性比![]() 的弱______。
的弱______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com