
| A. | 0.1mol NH3溶于足量水中(不考慮氨氣揮發),溶液中N原子的數目為0.1NA | |
| B. | 標準狀況下,22.4LNO與CO2的混合氣體中含有O原子數為3NA | |
| C. | 58.5 g的NaCl固體中含有NA個氯化鈉分子 | |
| D. | 0.1molN2與足量的H2反應,轉移的電子數是0.6NA |
分析 A.依據氮原子個數守恒解答;
B.依據n=$\frac{V}{22.4}$計算物質的量,采用極值分析判斷所含氧原子數;
C.氯化鈉為離子晶體,不含分子;
D.合成氨的反應為可逆反應.
解答 解:A.0.1mol NH3溶于足量水,依據氮原子個數守恒可知,溶液中N原子的數目為0.1NA,故A正確;
B.標準狀況下,22.4L NO與CO2的混合氣體物質的量為1mol,含有O的原子數為NA~2NA之間,故B錯誤;
C.氯化鈉為離子晶體,不含分子,故C錯誤;
D.合成氨的反應為可逆反應,不能進行徹底,故充分反應后轉移電子的數目小于0.6NA.故D錯誤;
故選:A.
點評 本題考查了阿伏伽德羅常數的有關計算,掌握公式的使用和物質的結構、可逆反應的特點是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 氧化性強弱順序是:Fe3+>Cl2>I2>SO42- | |
| B. | 還原性強弱順序是:SO2>I->Fe2+>Cl- | |
| C. | 反應Cl2+SO2+2H2O═2HCl+H2SO4不能發生 | |
| D. | Fe3+與I-在溶液可以大量共存 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向某溶液中滴加KSCN溶液,若溶液出現血紅色則說明原溶液中含Fe3+ | |
| B. | 向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,則說明原溶液中一定含Ag+ | |
| C. | 向某溶液中滴加足量稀HCl,產生氣體能使澄清石灰水變渾濁,則說明原溶液中一定含CO32- | |
| D. | 向某溶液中滴加NaOH溶液,除溶液體積增大外,無其它現象,說明該溶液與NaOH溶液不反應. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | x的原子半徑大于y的原子半徑 | |
| B. | x的電負性大于y的電負性 | |
| C. | x的核電荷數大于y的核電荷數 | |
| D. | x的第一電離能小于y 的第一電離能 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 實驗步驟 | 預期現象和結論 |
| 步驟1: | |
| 步驟2: | |
| 步驟3: |
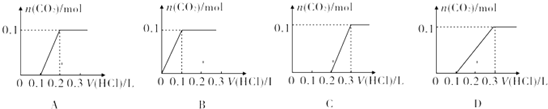
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
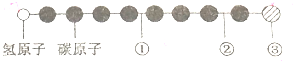 據報道,近來發現了一種新的星際分子,其分子模型如圖所示(途中給球與球之間的連線代表化學鍵,如單鍵、雙鍵、三鍵等,顏色相同的球表示同一種原子).下列對該物質的說法中正確的是( )
據報道,近來發現了一種新的星際分子,其分子模型如圖所示(途中給球與球之間的連線代表化學鍵,如單鍵、雙鍵、三鍵等,顏色相同的球表示同一種原子).下列對該物質的說法中正確的是( )| A. | ①處的化學鍵表示碳碳雙鍵 | B. | 此星際分子屬于烴類 | ||
| C. | ③處的原子可能是氯原子或氟原子 | D. | ②處的化學鍵表示碳碳單鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com