
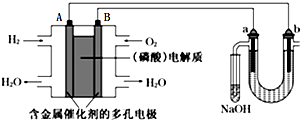
| A. | 電池工作時,B極反應式為O2+2H2O+4e-=4OH- | |
| B. | 電解時,電子流動路徑是:A極→外電路→b極→溶液→a極→B極 | |
| C. | NaOH溶液充分吸收后所得溶液可制作漂白水 | |
| D. | 當電池中消耗2.24L(標準狀況)H2時,a極周圍也會產生2.24L(標準狀況)氣體 |
分析 A、氫氧燃料電池中,正極上放電的是氧氣;
B、電子在導線中移動,不能在溶液中移動;
C、還原性:Br->Cl-,還原性強的離子在陽極先放電,氫氧化鈉溶液吸收電解時產生的氣體;
D、燃料電池和電解池中轉移的電子數是相等的.
解答 解:A、氫氧燃料電池中,正極上放電的是氧氣,在酸性電解質環境下,電極反應式為:O2+4H++4e-═2H2O,故A錯誤;
B、電子在導線中移動,不能在溶液中移動,故B錯誤;
C、還原性強的離子在陽極先放電,電解時,a電極周圍首先放電的是Br-后放電的為Cl-,所以試管中NaOH溶液是用來吸收電解時產生的溴蒸氣和氯氣,生成的溶液都具有強氧化性,具有漂白性,故C正確;
D、燃料電池和電解池中轉移的電子數是相等的,當電池中消耗2.24L(標準狀況)H2,根據電極反應:H2→2H++2e-,所以轉移電子$\frac{2.24L}{22.4L/mol}$×2=0.02mol,a極的電極反應為:2Br--2e-→Br2,轉移電子0.02mol,會產生0.01molBr2,Br2標準狀況下為液態,故D錯誤.
故選C.
點評 本題考查學生原電池和電解池的工作原理,要求學生熟記教材知識,學以致用.


科目:高中化學 來源: 題型:選擇題
 為了探索外界條件對反應2NO2(g)?N2O4(g)△H=-57kJ•mol-1的影響,若保持氣體總質量不變,在溫度為T1、T2時,通過實驗得到平衡體系中NO2的體積分數隨壓強變化曲線,實驗結果如圖所示.下列說法正確的是( )
為了探索外界條件對反應2NO2(g)?N2O4(g)△H=-57kJ•mol-1的影響,若保持氣體總質量不變,在溫度為T1、T2時,通過實驗得到平衡體系中NO2的體積分數隨壓強變化曲線,實驗結果如圖所示.下列說法正確的是( )| A. | a、c兩點氣體的平均相對分子質量:a>c | |
| B. | a、c兩點氣體的顏色:a淺,c深 | |
| C. | b、c兩點的平衡常數:Kb=Kc | |
| D. | 狀態a通過升高溫度可變成狀態b |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
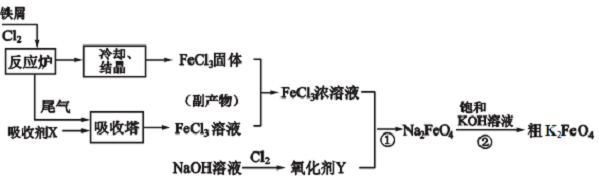
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗目的 | 實驗方案 |
| A | 檢驗CH3CH2Br與NaOH溶液是否發生反應 | 將CH3CH2Br與NaOH溶液共熱,冷卻,取上層溶液,加AgNO3溶液,觀察是否產生淡黃色沉淀 |
| B | 將打磨過的Al片投到一定濃度的CuCl2溶液,出現氣泡并有固體生成,過濾,向固體中加入過量的氨水,固體部分溶解 | Al與CuCl2溶液反應,有H2和Cu(OH)2生成 |
| C | 檢驗Fe(NO3)2晶體是否已氧化變質 | 將Fe(NO3)2樣品溶于稀H2SO4后,滴加KSCN溶液,觀察溶液是否變成紅色 |
| D | 檢驗乙醇與濃硫酸共熱是否產生乙烯 | 將乙醇與濃硫酸共熱至170℃,所得氣體通入酸性高錳酸鉀溶液中,觀察溶液是否褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
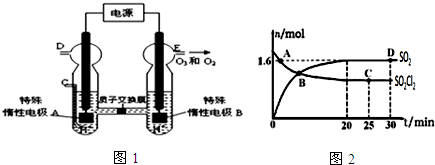
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用氯水、KSCN溶液檢驗FeCl3溶液中是否有FeCl2 | |
| B. | 用酸性高錳酸鉀溶液檢驗FeCl3溶液中是否有FeCl2 | |
| C. | 用NaOH溶液檢驗MgCl2溶液中是否有FeCl2 | |
| D. | 用硝酸檢驗某黃色固體是黃銅還是純銅 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molNa2O2晶體中陰離子的個數為2NA | |
| B. | 標準狀況下,2.24L苯所含的分子總數為0.1NA | |
| C. | 32gO2和32g O3的所含的氧原子數都是為2NA | |
| D. | 6.4g銅與過量的濃硝酸完全反應轉移的電子數是0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
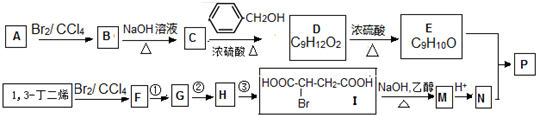
 ,
,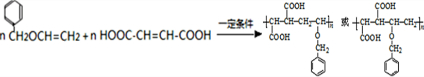 高聚物P的親水性比由E形成的聚合物強(填“強、弱”).
高聚物P的親水性比由E形成的聚合物強(填“強、弱”).
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com