
| 選項 | 實驗目的 | 實驗方案 |
| A | 檢驗CH3CH2Br與NaOH溶液是否發生反應 | 將CH3CH2Br與NaOH溶液共熱,冷卻,取上層溶液,加AgNO3溶液,觀察是否產生淡黃色沉淀 |
| B | 將打磨過的Al片投到一定濃度的CuCl2溶液,出現氣泡并有固體生成,過濾,向固體中加入過量的氨水,固體部分溶解 | Al與CuCl2溶液反應,有H2和Cu(OH)2生成 |
| C | 檢驗Fe(NO3)2晶體是否已氧化變質 | 將Fe(NO3)2樣品溶于稀H2SO4后,滴加KSCN溶液,觀察溶液是否變成紅色 |
| D | 檢驗乙醇與濃硫酸共熱是否產生乙烯 | 將乙醇與濃硫酸共熱至170℃,所得氣體通入酸性高錳酸鉀溶液中,觀察溶液是否褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.CH3CH2Br與NaOH溶液發生水解反應,檢驗溴離子應在酸性溶液中;
B.CuCl2溶液水解顯酸性,Al與水解產生的氫離子反應生成氫氣;
C.已氧化變質混有鐵離子,但樣品溶于稀H2SO4后,亞鐵離子、氫離子、硝酸根離子發生氧化還原反應生成鐵離子;
D.乙醇易揮發,乙醇、乙烯均能被高錳酸鉀氧化.
解答 解:A.CH3CH2Br與NaOH溶液發生水解反應,檢驗溴離子應在酸性溶液中,應水解后、冷卻加酸至酸性,再加AgNO3溶液,觀察是否產生淡黃色沉淀,故A錯誤;
B.CuCl2溶液水解顯酸性,Al與水解產生的氫離子反應生成氫氣,則促進銅離子水解生成Cu(OH)2,故B正確;
C.已氧化變質混有鐵離子,但樣品溶于稀H2SO4后,亞鐵離子、氫離子、硝酸根離子發生氧化還原反應生成鐵離子,則不能溶于酸,應溶于水滴加KSCN溶液,觀察溶液是否變成紅色,故C錯誤;
D.乙醇易揮發,乙醇、乙烯均能被高錳酸鉀氧化,應除去乙醇的干擾再檢驗乙烯,故D錯誤;
故選B.
點評 本題考查化學實驗方案的評價,為高頻考點,涉及有機物的結構與性質、鹽類水解、氧化還原反應、物質檢驗等,把握物質的性質、反應原理為解答的關鍵,側重分析與實驗能力的考查,綜合性較強,題目難度不大.


科目:高中化學 來源: 題型:選擇題
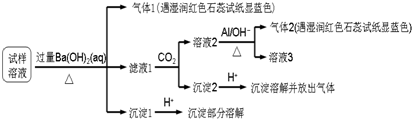
| A. | 試樣中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 試樣中可能含有Al3+ | |
| C. | 該霧霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| D. | 試樣中不可能存在Na+、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
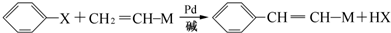
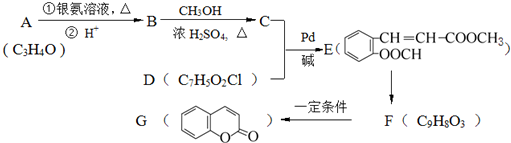

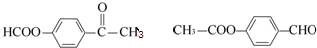
 )常用作香豆素的替代品.鑒別二氫香豆素和它的一種同分異構體(
)常用作香豆素的替代品.鑒別二氫香豆素和它的一種同分異構體( )需要用到的試劑有:NaOH溶液、稀硫酸、氯化鐵溶液
)需要用到的試劑有:NaOH溶液、稀硫酸、氯化鐵溶液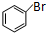 +CH2═CHCOOCH3$→_{堿}^{Pd}$
+CH2═CHCOOCH3$→_{堿}^{Pd}$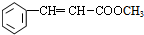 +HBr.
+HBr.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 纖維素可以水解生成葡萄糖,因此纖維素屬于基本營養物質 | |
| B. | 戊烷(C5H12)有兩種同分異構體 | |
| C. | 苯、溴苯、乙醇可以用水鑒別 | |
| D. | 乙醇可以直接氧化成乙酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | SO3、NO3-、BF3都是平面三角型 | B. | P4、CS2、PH3都是非極性分子 | ||
| C. | 金剛石、石墨、SiC都是原子晶體 | D. | 第一電離能:N>O>C |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
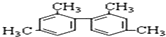
| A. | 等質量的該烴和甲烷均完全燃燒,耗氧量前者小于后者 | |
| B. | 該烴能使酸性高錳酸鉀溶液褪色,屬于苯的同系物 | |
| C. | 分子中一定有11個碳原子處于同一平面上 | |
| D. | 該烴的一氯取代產物為5種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
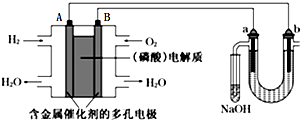
| A. | 電池工作時,B極反應式為O2+2H2O+4e-=4OH- | |
| B. | 電解時,電子流動路徑是:A極→外電路→b極→溶液→a極→B極 | |
| C. | NaOH溶液充分吸收后所得溶液可制作漂白水 | |
| D. | 當電池中消耗2.24L(標準狀況)H2時,a極周圍也會產生2.24L(標準狀況)氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 葡萄糖氯化鈉注射液--用于補充熱能和體液 | |
| B. | 二氧氯(ClO2)或漂白粉--利用其氧化性對居所和飲用水消毒 | |
| C. | 絡合碘--碘化鉀的水溶液,可以用于皮膚和粘膜的消毒 | |
| D. | 電池--通常選用干電池,用于小功率電器的供電 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 溶液中一定不存在CO32- | B. | 溶液中一定不存在Fe3+ | ||
| C. | 溶液中一定存在K+ | D. | 溶液中c(NO3-)=0.1mol/L |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com