
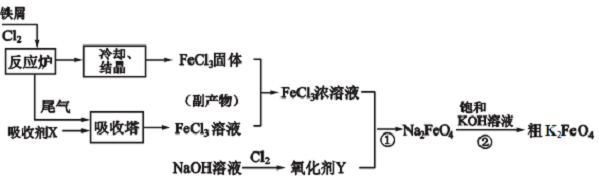
分析 鐵與氯氣反應生成紅棕的煙,過量的氯氣用氯化亞鐵溶液吸收,生成氯化鐵溶液,紅棕色氯化鐵用氯化鐵溶液吸收,生成濃的氯化鐵溶液,然后氯化鐵被氯氣與氫氧化鈉溶液反應生成的次氯酸鈉氧化成高鐵酸鈉,最后通過反應2KOH+Na2FeO4=K2FeO4+2NaOH,制得高鐵酸鉀,由此分析解答:
(1)從反應爐中排出的尾氣是反應剩余的Cl2,與吸收劑X反應生成FeCl3溶液,所以X是氯化亞鐵溶液;防止鐵離子的水解,所以要加入鹽酸;
(2)首先加入過量的鐵粉將鐵離子轉化為亞鐵離子,銅離子轉化為單質銅,然后加入適量的鹽酸除去過量的鐵粉,最后過濾得到單質銅;
(3)氫氧化鈉與氯氣反應生成NaClO,次氯酸鈉與FeCl3反應生成FeO42-;
(4)過程②將混合溶液攪拌半小時,靜置,抽濾獲得粗產品.該反應的化學方程式為2KOH+Na2FeO4 =K2FeO4+2NaOH,請根據相關反應原理分析反應能發生的原因K2FeO4的溶解度比Na2FeO4小而溶液中K+、FeO42-的濃度比較大;K2FeO4 在水溶液中易發生反應:4FeO42-+10H2O═4Fe(OH)3+8OH-+3O2↑,所以用堿液來洗滌,抑制水解,不引入新的雜質所以用稀KOH溶液,異丙醇易揮發.
解答 解:(1)通過工藝流程圖可知,從反應爐中排出的尾氣是反應剩余的Cl2,與吸收劑X在吸收塔中反應生成FeCl3溶液,則吸收劑X應是FeCl2溶液,防止鐵離子的水解,所以要加酸,而不引入新的雜質,所以加鹽酸,故答案為:FeCl2;加入少量鹽酸(或通入HCl);
(2)首先加入過量的鐵粉將鐵離子轉化為亞鐵離子,銅離子轉化為單質銅,然后加入適量的鹽酸除去過量的鐵粉,最后過濾得到單質銅,故答案為:Fe(鐵屑)、HCl(鹽酸);
(3)NaClO與FeCl3反應生成FeO42-、次氯酸鈉被還原為氯離子,則反應的離子方程式為:2Fe3++3ClO-+10OH-═2FeO42-+3Cl-+5H2O;
故答案為:2Fe3++3ClO-+10OH-═2FeO42-+3Cl-+5H2O;
(4)過程②將混合溶液攪拌半小時,靜置,抽濾獲得粗產品.該反應的化學方程式為2KOH+Na2FeO4 =K2FeO4+2NaOH,請根據相關反應原理分析反應能發生的原因K2FeO4的溶解度比Na2FeO4小而溶液中K+、FeO42-的濃度比較大;K2FeO4 在水溶液中易發生反應:4FeO42-+10H2O═4Fe(OH)3+8OH-+3O2↑,所以用堿液來洗滌,抑制水解,不引入新的雜質所以用稀KOH溶液,異丙醇易揮發,故答案為:K2FeO4溶解度小,析出晶體,促進反應進行;b.
點評 本題考查了物質的制備流程的理解應用、實驗基本操作、物質性質的分析應用,題目涉及的知識點較多,側重于考查學生的實驗能力和對基礎知識的綜合應用能力,熟練掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
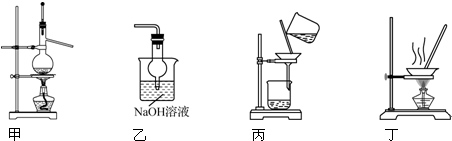
| A. | 用裝置甲以乙醇和濃硫酸為原料制乙烯 | |
| B. | 用裝置乙吸收某些實驗尾氣中的二氧化硫 | |
| C. | 用裝置丙分離Cl2與KI溶液反應生成的碘 | |
| D. | 用裝置丁蒸干NH4Cl飽和溶液獲取NH4Cl晶體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


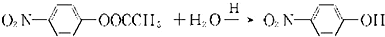 +CH3COOH.
+CH3COOH.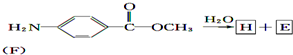
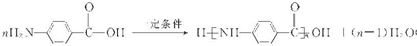 .
.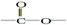 結構.
結構. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
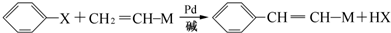
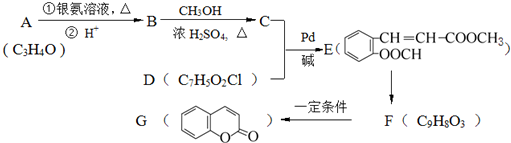

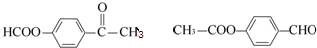
 )常用作香豆素的替代品.鑒別二氫香豆素和它的一種同分異構體(
)常用作香豆素的替代品.鑒別二氫香豆素和它的一種同分異構體( )需要用到的試劑有:NaOH溶液、稀硫酸、氯化鐵溶液
)需要用到的試劑有:NaOH溶液、稀硫酸、氯化鐵溶液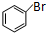 +CH2═CHCOOCH3$→_{堿}^{Pd}$
+CH2═CHCOOCH3$→_{堿}^{Pd}$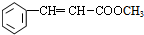 +HBr.
+HBr.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 事實 | 解釋 |
| A | 用熱的純堿溶液洗去油污 | Na2CO3可作為油脂分解的催化劑 |
| B | 鋁罐車可用于運輸稀硝酸 | 鋁表面形成致密氧化膜具有保護作用 |
| C | 甘油作為化妝品中的保濕劑 | 甘油易與水形成氫鍵 |
| D | 氫氟酸刻蝕水晶工藝品 | HF具有強酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 纖維素可以水解生成葡萄糖,因此纖維素屬于基本營養物質 | |
| B. | 戊烷(C5H12)有兩種同分異構體 | |
| C. | 苯、溴苯、乙醇可以用水鑒別 | |
| D. | 乙醇可以直接氧化成乙酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | SO3、NO3-、BF3都是平面三角型 | B. | P4、CS2、PH3都是非極性分子 | ||
| C. | 金剛石、石墨、SiC都是原子晶體 | D. | 第一電離能:N>O>C |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
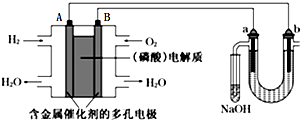
| A. | 電池工作時,B極反應式為O2+2H2O+4e-=4OH- | |
| B. | 電解時,電子流動路徑是:A極→外電路→b極→溶液→a極→B極 | |
| C. | NaOH溶液充分吸收后所得溶液可制作漂白水 | |
| D. | 當電池中消耗2.24L(標準狀況)H2時,a極周圍也會產生2.24L(標準狀況)氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 該溶液中氫離子的濃度:c(H+)=1×10-11 mol•L-1 | |
| B. | pH=7 的NH4Cl和NH3•H2O的混合溶液:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | 濃度均為0.1 mol•L-1的NH3•H2O和NH4Cl溶液等體積混合后的堿性溶液中:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1的氨水與0.05 mol•L-1的 H2SO4溶液等體積混合后所得溶液中:2c(NH4+)+2c(NH3•H2O)=c(SO42-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com