
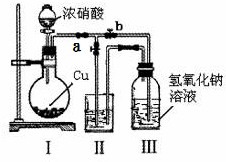
 針對網絡上流傳的隔夜熟肉中因亞硝酸鈉(NaNO2)含量嚴重超標而不能食用的說法,某興趣小組開展如下探究活動:
針對網絡上流傳的隔夜熟肉中因亞硝酸鈉(NaNO2)含量嚴重超標而不能食用的說法,某興趣小組開展如下探究活動:分析 (1)NaNO2為強堿弱酸鹽,亞硝酸根離子能發生水解;
(2)NaNO2有氧化性,能將碘離子氧化成碘單質,據此答題;
(3)①裝置II為尾氣吸收裝置,二氧化氮與水反應生成一氧化氮,還是能污染空氣;
②裝置III中反應完全后,要將裝置中的二氧化氮用裝置II吸收,所以要先打開a,再關閉b;
(4)將NaNO2溶液露置于空氣中,能被空氣中的氧化氧化成硝酸鈉,亞硝酸根水解產生的氫氧根離子減少,所以溶液的pH減小,據此答題;
(5)①根據氧化還原滴定的操作可確定所用儀器;
②因為高錳酸鉀的稀溶液是紅色的,所以滴定終點時,溶液會出現紅色;
③根據電子得失守恒可知關系式2KMnO4~5NaNO2,由關系式根據消耗的高錳酸鉀溶液的物質的量可計算出亞硝酸鈉的質量,進而確定隔夜熟肉中NaNO2的含量,并據此判斷能否食用.
解答 解:(1)NaNO2為強堿弱酸鹽,亞硝酸根離子能發生水解,水解的離子方程式為NO2-+H2O?HNO2+OH-,
故答案為:NO2-+H2O?HNO2+OH-;
(2)NaNO2有氧化性,能將碘離子氧化成碘單質,所以要酸性條件下,NaNO2能使淀粉、KI溶液變藍,
故答案為:NaNO2;
(3)①Ⅰ裝置中產生的二氧化氮,與水反應能產生一氧化氮,排到空氣中會造成污染,所以水不能作為裝置Ⅱ中的試劑,
故答案為:二氧化氮與水反應能產生一氧化氮,排到空氣中會造成污染;
②裝置III中反應完全后,要將裝置中的二氧化氮用裝置II吸收,所以要先打開a,再關閉b,
故答案為:a;b;
(4)將NaNO2溶液露置于空氣中,能被空氣中的氧化氧化成硝酸鈉,溶液中NaNO2的含量,亞硝酸根水解產生的氫氧根離子減少,所以溶液的pH減小,反應的化學方程式為2NaNO2+O2=2NaNO3,
故答案為:減少;2NaNO2+O2=2NaNO3;
(5)①根據氧化還原滴定的操作可知,用到的儀器為酸式滴定管、錐形瓶,故選BE,
故答案為:BE;
②因為高錳酸鉀的稀溶液是紅色的,所以滴定終點時,溶液會出現紅色,所以滴定終點的判斷依據為:滴入最后一滴標準液時錐形瓶內溶液變紅,且30秒內不褪色,
故答案為:滴入最后一滴標準液時錐形瓶內溶液變紅,且30秒內不褪色;
③根據題意可知,與隔夜熟肉中提取的NaNO2反應的KMnO4的物質的量為0.00500mol/L×0.016L=8.0×10-5 mol,根據電子得失守恒可知關系式2KMnO4~5NaNO2,由關系式可知亞硝酸鈉的質量為$\frac{5}{2}$×8.0×10-5 mol×69g/mol=13.8mg,所以隔夜熟肉中NaNO2的含量為$\frac{13.8mg}{1kg}$=13.8mg/Kg<30mg/kg,所以能食用,
故答案為:13.8;能.
點評 本題主要考查實驗基本操作和實驗原理的應用分析,中等難度,答題時注意把元素化合物知識與實驗原理充分結合,注意化學用語的正確書寫.


科目:高中化學 來源: 題型:選擇題
| A. | 同溫度下,CuS的溶解度大于ZnS的溶解度 | |
| B. | 將足量CuSO4溶解在0.1 mol•L-1的H2S溶液中,Cu2+能達到的最大濃度為1.3×10-35 mol•L-1 | |
| C. | 因為H2SO4是強酸,故CuSO4+H2S═CuS↓+H2SO4不能發生 | |
| D. | 除去工業廢水中的Cu2+,可以選用FeS作沉淀劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Zn和濃H2SO4 | B. | C和濃HNO3 | ||
| C. | Cu和濃HNO3 | D. | Na2O2和NH4Cl濃溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Z為0.3 | B. | Y2為0.4 | C. | X2為0.2 | D. | Z為0.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某溶液中由水電離出的c(H+)=1×10-amol•L-1,若a>7時,則該溶液的pH一定為14-a | |
| B. | 將0.2mol•L-1的某一元酸HA溶液和0.1mol•L-1的NaOH溶液等體積混合后溶液的pH大于7,則反應后的混合液:c(HA)>c(A-) | |
| C. | Na2CO3溶液:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 常溫下NaHSO3溶液的pH<7,溶液中c(SO32-)<c(H2SO3) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在其它條件相同時,將等質量的鋅塊和鋅粉與相同濃度的鹽酸反應,鋅粉反應快 | |
| B. | 將質量相同、形狀大小一樣的鋁條分別與稀硫酸和濃硫酸反應,濃硫酸產生氫氣快 | |
| C. | 兩支試管中分別加入雙氧水,其中一支試管中再加入少量二氧化錳,同時加熱,產生氧氣的快慢不同 | |
| D. | 在稀硫酸和鐵粉反應制取氫氣時,加入適量醋酸鈉晶體,可減慢反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 類型 | 離子化合物 | 離子化合物 | 離子化合物 | 共價化合物 |
| 熔點/℃ | 2800 | 2050 | 714 | 191 |
 ;在上述由SiCl4制純硅的反應中,測得每生成1.12kg純硅需吸收akJ熱量,寫出該反應的熱化學方程式2H2(g)+SiCl4(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025akJ•mol-1.
;在上述由SiCl4制純硅的反應中,測得每生成1.12kg純硅需吸收akJ熱量,寫出該反應的熱化學方程式2H2(g)+SiCl4(g)$\frac{\underline{\;1100℃\;}}{\;}$Si(s)+4HCl(g)△H=+0.025akJ•mol-1.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 油脂是天然高分子化合物 | |
| B. | 蔗糖和麥芽糖互為同分異構體 | |
| C. | 蛋白質溶液中加入Na2SO4可使其變性 | |
| D. | 苯酚、甲醛通過加聚反應可制得酚醛樹脂 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com