
| A. | 120mL | B. | 150mL | C. | 200mL | D. | 220mL |
分析 再逐滴加入1mol/L NaOH溶液,若滴加NaOH溶液體積至80mL時,溶液中始終未產生沉淀,然后繼續滴加NaOH溶液則開始出現沉淀,說明硫酸有剩余,據此可計算出金屬消耗硫酸的物質的量,然后列式計算出鎂、鋁的物質的量;當沉淀的質量不再變化時,溶質為偏鋁酸鈉和硫酸鈉,結合質量守恒定律計算出消耗氧化鈉的物質的量,進而計算需要氫氧化鈉溶液體積.
解答 解:“若滴加NaOH溶液體積至80mL時,溶液中始終未產生沉淀,然后繼續滴加NaOH溶液則開始出現沉淀”,說明硫酸有剩余,
80mL 1mol/L的氫氧化鈉溶液中含有氧化鈉的物質的量為:1mol/L×0.08L=0.08mol,0.08mol氧化鈉消耗硫酸的物質的量為:0.08mol×$\frac{1}{2}$=0.04mol,
則0.05mol鎂和鋁總共消耗硫酸的物質的量為:1mol/L×0.1L-0.04mol=0.06mol,
設混合物中含有Mg、鋁的物質的量分別為x、y,
則:x+y=0.05、x+1.5y=0.06,解得:x=0.03mol、y=0.02mol,
當溶液中沉淀質量不再發生變化時,此時溶質為偏鋁酸鈉和硫酸鈉,根據質量守恒定律可知:n(Na2SO4)=n(H2SO4)、n(NaAlO2)=n(Al),
故n(NaOH)=2n(Na2SO4)+n(NaAlO2)=n(Al)+2n(H2SO4)=2×0.1L×1mol/L+0.02mol=0.22mol,
所以需要氫氧化鈉溶液的體積為:$\frac{0.22mol}{1mol/L}$=0.22L=220mL,
故選D.
點評 本題考查了混合物反應的計算,題目難度中等,明確發生反應的實質為解答關鍵,注意掌握質量守恒定律在化學計算中的應用,試題培養了學生的化學計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 溶液中加水,$\frac{c(HC{O}_{3}^{-})•c(O{H}^{-})}{c(C{O}_{3}^{2-})}$增大 | |
| B. | 加入Na2CO3固體,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$減小 | |
| C. | 升高溫度,平衡常數減小 | |
| D. | 通入CO2,溶液pH增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石油、煤、天然氣、油脂都屬于化石燃料 | |
| B. | 油脂在堿性條件下的水解反應又稱為皂化反應 | |
| C. | 分子式為(C6H10O5)n的淀粉和纖維素互為同分異構 | |
| D. | 蔗糖是還原性糖 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 17g NH3所含的電子數是 10NA | |
| B. | 常溫常壓下,22.4L氧氣含氧原子數為2NA | |
| C. | 5.6g鐵粉與足量Cl2反應,失去的電子數為0.2NA | |
| D. | 2.3g金屬鈉全部變成鈉離子時失去的電子數是0.2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相同條件下NaHCO3比Na2CO3更 穩定 | |
| B. | 向等量的Na2CO3和NaHCO3固體中分別滴加同濃度的鹽酸,后者產生氣泡速率快 | |
| C. | 相同條件下NaHCO3比Na2CO3更易溶于水 | |
| D. | 經實驗測定,Na2CO3溶液顯堿性,說明Na2CO3屬于堿 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向NaAlO2溶液中通入過量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| B. | 用氯化鐵溶液腐蝕銅板:Fe3++Cu═Cu2++Fe2+ | |
| C. | 氯化鋁溶液中加入過量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | Fe3O4與足量稀HNO3反應:3Fe3O4+28H++NO3-═9Fe3++NO↑+14H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
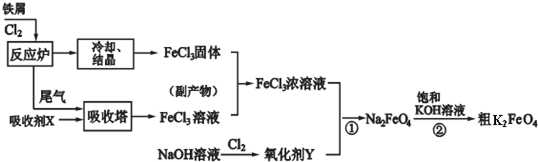
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
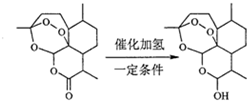
| A. | 青蒿素分子中治療瘧疾的活性基團是過氧基 | |
| B. | 雙氫青蒿素分子比青蒿素分子多1個手性碳原子 | |
| C. | 理論上每摩爾青蒿素水解需要消耗1molNaOH | |
| D. | 每摩爾雙氫青蒿素可以與1molNaHCO3反應生成1molCO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com