
| A. | 28 g鐵粉與酸反應失去的電子數是NA | |
| B. | 標準狀況下,11.2 L NH3含有的原子總數為1.5NA | |
| C. | 0.5 mol•L-1 K2SO4溶液中所含K+的數目為NA | |
| D. | 46 g N02和N2O4的混合氣體含有的原子總數為3NA |
分析 A.鐵與氧化性酸反應生成三價鐵離子,與非氧化性酸反應生成二價鐵離子;
B.氨氣為四原子分子;
C.溶液體積未知;
D.NO2和N2O4最簡式相同為NO2,計算46gNO2中所含原子數.
解答 解:A.鐵與酸反應轉移電子數,與酸的類型與酸的用量有關,例如與足量硝酸反應生成硝酸鐵,與少量硝酸反應生成硝酸亞鐵,鹽酸與鐵反應生成氯化亞鐵,所以酸的類型、用量不確定,無法計算轉移電子數,故A錯誤;
B.標準狀況下,11.2 L NH3含有的原子總數為$\frac{11.2L}{22.4L/mol}$×4×NA=2NA,故B錯誤;
C.依據n=CV,溶液體積未知,無法計算硫酸鉀的物質的量,無法計算鉀離子個數,故C錯誤;
D.NO2和N2O4最簡式相同為NO2,計算46gNO2中所含原子數$\frac{46g}{46g/mol}$×3×NA=3NA,故D正確;
故選:D.
點評 本題考查了阿伏伽德羅常數的分析應用,掌握好以物質的量為中心的各化學量與阿伏加德羅常數的關系,明確氣體摩爾體積的條件應用是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:解答題
| 弱酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 電離平衡常數(25℃) | Ka=1.77×10-4 | Ka=4.0 ×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑的大小順序:W>X>Y | |
| B. | W的簡單氣態氫化物的熱穩定性比Y的弱 | |
| C. | Z分別與Q、X形成的化合物中化學鍵類型相同 | |
| D. | X的最高價氧化物對應水化物的堿性在同周期中最強 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
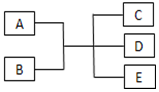 已知A、B、C、D、E是化學中常見的物質,常溫下,E是一種無色無味的液體,它們之間有如圖反應關系.
已知A、B、C、D、E是化學中常見的物質,常溫下,E是一種無色無味的液體,它們之間有如圖反應關系.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 泡沫滅火器的反應原理是非氧化還原反應 | |
| B. | 鋼鐵析氫腐蝕和吸氧腐蝕的速率一樣快 | |
| C. | 鍋爐水垢中含有的CaSO4,可先用Na2CO3溶液處理,后用酸除去 | |
| D. | 燃料電池的燃料都在負極發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 14 g乙烯氣體中的氫原子數約為2×6.02×1023 | |
| B. | 標準狀況下,2.24 L H2O含有的共價鍵數約為0.2×6.02×1023 | |
| C. | 1 mol N2與3 mol H2反應生成的NH3分子數約為2×6.02×1023 | |
| D. | 0.1 L 0.5 mol/L CH3COOH溶液中含有的氫離子數約為0.05×6.02×1023 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu2+為重金屬離子,故CuSO4不能用于生活用水消毒 | |
| B. | 鹵水煮豆腐是Mg2+、Ca2+等使蛋白質膠體發生凝聚過程 | |
| C. | 純堿溶液可以洗滌餐具上的油漬 | |
| D. | 油漆刷在鋼鐵護欄表層用來防止金屬銹蝕 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com