

分析 (1)常溫下,鐵和濃硫酸發生鈍化現象;
(2)①亞鐵離子具有還原性,能被酸性高錳酸鉀溶液氧化而使酸性高錳酸鉀溶液褪色;
②根據SO2+Br2+2H2O═2HBr+H2SO4知,二氧化硫被氧化生成硫酸,硫酸和氯化鋇反應生成硫酸鋇沉淀,所以2.33g沉淀是BaSO4,n(BaSO4)=$\frac{2.33g}{233g/mol}$=0.01mol,根據S原子守恒得n(BaSO4)=n(S)=n(SO2)=0.01mol,標況下二氧化硫體積=0.01mol×22.4L/mol=224mL;
(3)品紅溶液能檢驗二氧化硫存在;
(4)碳和濃硫酸反應生成二氧化碳,所以Q為CO2,二氧化硫和二氧化碳都能使澄清石灰水變渾濁,所以應該在排除二氧化硫條件下將氣體通入澄清石灰水中檢驗二氧化碳;
(5)氫氣具有還原性,在加熱條件下,能將黑色的CuO還原為紅色的Cu,且生成水,水能使無水硫酸銅變藍色;
(6)空氣中含有水蒸氣和二氧化碳,影響氫氣、二氧化碳的檢驗.
解答 解:(1)常溫下,鐵和濃硫酸反應生成一層致密的氧化物薄膜而阻止進一步被氧化,該現象為鈍化現象,所以將鐵釘放入濃硫酸片刻無明顯變化的原因是鐵釘表面被鈍化,故答案為:鐵釘表面被鈍化(或其他合理答案);
(2)①a.氯水能將亞鐵離子氧化為鐵離子,鐵離子和KSCN溶液反應導致溶液呈血紅色,但不能確定原來溶液中一定含有亞鐵離子,故錯誤;
b.鐵粉和酸反應生成亞鐵離子,不能確定原來溶液中是否含有亞鐵離子,故錯誤;
c.濃氨水和亞鐵離子反應生成氫氧化亞鐵沉淀,氫氧化亞鐵能被氧化生成氫氧化鐵紅褐色沉淀,不能確定溶液中一定含有亞鐵離子,故錯誤;
d.亞鐵離子具有還原性,能被酸性高錳酸鉀溶液氧化而使酸性高錳酸鉀溶液褪色,所以可以用酸性高錳酸鉀溶液檢驗亞鐵離子,故正確;
故選d;
②根據SO2+Br2+2H2O═2HBr+H2SO4知,二氧化硫被氧化生成硫酸,硫酸和氯化鋇反應生成硫酸鋇沉淀,所以2.33g沉淀是BaSO4,n(BaSO4)=$\frac{2.33g}{233g/mol}$=0.01mol,根據S原子守恒得n(BaSO4)=n(S)=n(SO2)=0.01mol,標況下二氧化硫體積=0.01mol×22.4L/mol=224mL,二氧化硫體積分數=$\frac{224mL}{336mL}×100%$=66.7%,
故答案為:66.7%;
(3)品紅溶液能檢驗二氧化硫存在,所以該裝置的作用是檢驗SO2是否除盡,故答案為:檢驗SO2是否除盡;
(4)碳和濃硫酸反應生成二氧化碳,所以Q為CO2,二氧化硫和二氧化碳都能使澄清石灰水變渾濁,所以應該在排除二氧化硫條件下將氣體通入澄清石灰水中檢驗二氧化碳,故選c;
(5)氫氣具有還原性,在加熱條件下,能將黑色的CuO還原為紅色的Cu,且生成水,水能使無水硫酸銅變藍色,所以如果Y中含有氫氣,預計實驗現象是D中固體由黑變紅,E中固體由白變藍,故答案為:D中固體由黑變紅,E中固體由白變藍;
(6)空氣中含有水蒸氣和二氧化碳,影響氫氣、二氧化碳的檢驗,所以該裝置作用是防止空氣中的CO2和水蒸氣進入裝置E中,
故答案為:防止空氣中的CO2和水蒸氣進入裝置E中.
點評 本題考查性質實驗方案評價,為高頻考點,明確實驗原理是解本題關鍵,知道每個裝置可能發生的反應及其作用,難點是判斷堿石灰作用,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 共包含18種元素 | B. | 前3周期元素 | ||
| C. | 除稀有氣體外,Cl的原子半徑最大 | D. | 僅含5種金屬元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何晶體中都存在化學鍵 | |
| B. | 晶體內部的微粒在空間的排列均服從緊密堆積原理 | |
| C. | 任何晶體中,若有陰離子必定含有陽離子 | |
| D. | 金屬晶體的熔點都比分子晶體的熔點高 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
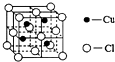 銅是過渡金屬元素,可以形成多種化合物.
銅是過渡金屬元素,可以形成多種化合物.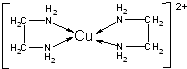
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
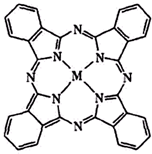 鋰亞硫酰氯(Li-SOCl2)電池具有能量密度高、工作電壓和放電電壓平穩、工作溫度范圍寬及貯存壽命長等優點,在航海、醫療及井下油田設備等方面的應用廣泛.
鋰亞硫酰氯(Li-SOCl2)電池具有能量密度高、工作電壓和放電電壓平穩、工作溫度范圍寬及貯存壽命長等優點,在航海、醫療及井下油田設備等方面的應用廣泛.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
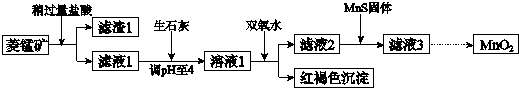
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 開始沉淀時 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀時 | 9.8 | 8.3 | 3.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
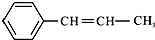 ,它可能具有的性質是( )
,它可能具有的性質是( )| A. | 不溶于水,易溶于有機溶劑 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| C. | 能發生聚合反應,其產物可表示為: | |
| D. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ①② |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
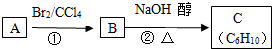
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com