
 在元素周期表前四周期原子序數依次增大的六種元素A、B、C、D、E、F中,A與其余五種元素既不同周期也不同主族,B的一種核素在考古時常用來鑒定一些文物的年代,C的氧化物是導致酸雨的主要物質之一,D原子核外電子有8種不同的運動狀態,E的基態原子在前四周期元素的基態原子中單電子數最多,F元素的基態原子最外能層只有一個電子,其它能層均已充滿電子.
在元素周期表前四周期原子序數依次增大的六種元素A、B、C、D、E、F中,A與其余五種元素既不同周期也不同主族,B的一種核素在考古時常用來鑒定一些文物的年代,C的氧化物是導致酸雨的主要物質之一,D原子核外電子有8種不同的運動狀態,E的基態原子在前四周期元素的基態原子中單電子數最多,F元素的基態原子最外能層只有一個電子,其它能層均已充滿電子. ; A2D由液態形成晶體時密度減小,其主要原因水形成晶體時,每個水分子與4個水分子形成氫鍵,構成空間正四面體網狀結構,水分子空間利用率低,密度反而減小(用文字敘述).
; A2D由液態形成晶體時密度減小,其主要原因水形成晶體時,每個水分子與4個水分子形成氫鍵,構成空間正四面體網狀結構,水分子空間利用率低,密度反而減小(用文字敘述).分析 在元素周期表前四周期中原子序數依次增大的六種元素A、B、C、D、E、F中,B的一種核素在考古時常用來鑒定一些文物的年代,則B為碳元素,D原子核外電子有8種不同的運動狀態,則D為氧元素,C的氧化物是導致酸雨的主要物質之一,且C的原子序數小于D,所以C為氮元素,E的基態原子在前四周期元素的基態原子中單電子數最多,其原子外圍電子排布式為1s22s22p63s23p63d54s1,則E為鉻元素,F元素的基態原子最外能層只有一個電子,其它能層均已充滿,則F原子外圍電子排布為3d104s1,所以F為銅元素,A與其余五種元素既不同周期也不同主族,所以A為氫元素,據此答題.
解答 解:在元素周期表前四周期中原子序數依次增大的六種元素A、B、C、D、E、F中,B的一種核素在考古時常用來鑒定一些文物的年代,則B為碳元素,D原子核外電子有8種不同的運動狀態,則D為氧元素,C的氧化物是導致酸雨的主要物質之一,且C的原子序數小于D,所以C為氮元素,E的基態原子在前四周期元素的基態原子中單電子數最多,其原子外圍電子排布式為1s22s22p63s23p63d54s1,則E為鉻元素,F元素的基態原子最外能層只有一個電子,其它能層均已充滿,則F原子外圍電子排布為3d104s1,所以F為銅元素,A與其余五種元素既不同周期也不同主族,所以A為氫元素.
(1)E為鉻元素,基態E原子的價電子排布為3d54s1,故答案為:3d54s1;
(2)C、O、N元素都是第二周期非金屬元素,同一周期元素自左而右第一電離能呈增大趨勢,但N元素原子2p能級是半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素,故第一電離能:C<O<N;
A與C形成NH3型分子,分子中N原子形成3個N-H、含有1對孤對電子,故N原子雜化類型為sp3,分子的立體結構為三角錐形;
C的單質為N2,化合物CO是等電子體,二者結構相似,CO分子中C原子與O原子之間形成三對共用電子對,故CO的電子式為 ;
;
H2O形成晶體時,每個水分子與4個水分子形成氫鍵,構成空間正四面體網狀結構,水分子空間利用率低,密度反而減小,
故答案為:C<O<N;sp3;三角錐形; ;水形成晶體時,每個水分子與4個水分子形成氫鍵,構成空間正四面體網狀結構,水分子空間利用率低,密度反而減小;
;水形成晶體時,每個水分子與4個水分子形成氫鍵,構成空間正四面體網狀結構,水分子空間利用率低,密度反而減小;
(3)根據晶胞的結構圖可知,晶胞中含有氧原子數為1+8×$\frac{1}{8}$=2,銅原子數為4,所以該化合物的化學式為Cu2O,晶胞質量為(4×$\frac{64}{{N}_{A}}$+2×$\frac{16}{{N}_{A}}$)g,若相鄰氧原子和銅原子間的距離為a cm,則晶胞的體對角線為4acm,所以邊長為$\frac{4a}{\sqrt{3}}$cm,所以體積為($\frac{4a}{\sqrt{3}}$)3cm3,該晶體的密度為(4×$\frac{64}{{N}_{A}}$+2×$\frac{16}{{N}_{A}}$)g÷($\frac{4a}{\sqrt{3}}$)3cm3=$\frac{27\sqrt{3}}{2{a}^{3}{N}_{A}}$g/cm3,
故答案為:Cu2O;$\frac{27\sqrt{3}}{2{a}^{3}{N}_{A}}$.
點評 本題是對物質結構的考查,涉及核外電子排布、電離能、雜化軌道、等電子體、氫鍵度物質性質的影響、晶胞的計算等,中等難度,元素推斷是解題的關鍵,需要學生具備扎實的基礎,(3)中注意利用均攤法計算晶胞質量,關鍵是計算晶胞體積.


科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{8}^{16}$O2和${\;}_{8}^{18}$O2互為同位素,物理性質有差異而化學性質相似 | |
| B. | N2與O2的反應屬于氮的固定 | |
| C. | 元素周期表中7個橫行分別是7個周期,18個縱行分別是18個族 | |
| D. | 1mol金剛石比1mol石墨燃燒放出熱量多,所以金剛石比石墨穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHCO3溶液加水稀釋,$\frac{c(N{a}^{+})}{c(HC{{O}_{3}}^{-})}$的比值保持增大 | |
| B. | 在0.1 mol•L一1氨水中滴加0.lmol•L一1鹽酸,恰好完全中和時溶液的pH<7 | |
| C. | 向0.lmol/L Na2S03溶液中加人少量NaOH固體,c(Na+)、c(SO32-)均增大 | |
| D. | 0.lmol•L一1氨水加水稀釋,溶液中c(H+)和c(OH-)都減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸與鋅反應放出氫氣多 | |
| B. | 醋酸與鋅反應速率小 | |
| C. | 鹽酸和醋酸分別與鋅反應放出的氫氣一樣多 | |
| D. | 鹽酸和醋酸分別與鋅反應的速率一樣大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ①②③ | C. | ②③④ | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 32 g | B. | 32 g/mol | C. | 34 g | D. | 34 g/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
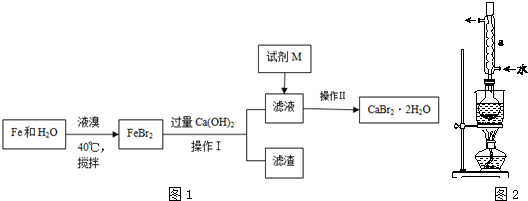
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com