
| A. | Ca(HCO3 )2與澄清石灰水反應可以表示為:2Ca2++3HCO${\;}_{3}^{-}$+3OH-═2CaCO3↓+CO${\;}_{3}^{2-}$+3H2O | |
| B. | 用Pt電極電解少量的CuC12溶液:2H2O+Cu2++2Cl-═H2↑+Cl2↑+Cu(OH)2↓ | |
| C. | 向CuSO4,溶液中加人Na2O2:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ | |
| D. | 向NaCIO和NaCI混合溶液中滴人少量FeSO4溶液:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O |
分析 A.碳酸氫鈣與氫氧化鈣反應生成碳酸鈣沉淀和水;
B.電解氯化銅溶液生成銅和氯氣;
C.硫酸銅溶液與過氧化鈉反應生成氫氧化銅、硫酸鈉和氧氣;
D.硫酸亞鐵少量,鐵離子與次氯酸根離子發生雙水解反應生成氫氧化鐵沉淀.
解答 解:A.Ca(OH)2與Ca(HCO3)2反應生成碳酸鈣沉淀和水,正確的離子反應為:Ca2++HCO3-+OH-=CaCO3↓+H2O,故A錯誤;
B.用Pt電極電解少量的CuC12溶液,反應生成銅和氯氣,正確的離子方程式為:Cu2++2Cl-═Cl2↑+Cu,故B錯誤;
C.向CuSO4溶液中加人Na2O2,反應生成硫酸鈉、氫氧化銅沉淀和氧氣,反應的離子方程式為:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑,故C正確;
D.NaClO為強堿弱酸鹽,水解呈堿性,NaCl為中性,溶液中不存在大量的氫離子,正確的離子方程式為:2Fe2++ClO-+H2O=Fe3++Fe(OH)3↓+Cl-,故D錯誤;
故選C.
點評 本題考查了離子方程式的判斷,為高考的高頻題,題目難度中等,注意掌握離子方程式正誤判斷常用方法:檢查反應物、生成物是否正確,檢查各物質拆分是否正確,如難溶物、弱電解質等需要保留化學式,檢查是否符合原化學方程式等.


科目:高中化學 來源: 題型:解答題
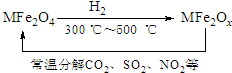 新型納米材料氧缺位鐵酸鹽MFe2Ox(3<x<4,M=Mn、Zn、Ni,且均為+2價,下同)是由鐵酸鹽MFe2O4經過高溫與H2反應制得.常溫下,它能使工業廢氣中的酸性氧化物(SO2、NO2等)轉化為其單質除去,轉化流程如圖:
新型納米材料氧缺位鐵酸鹽MFe2Ox(3<x<4,M=Mn、Zn、Ni,且均為+2價,下同)是由鐵酸鹽MFe2O4經過高溫與H2反應制得.常溫下,它能使工業廢氣中的酸性氧化物(SO2、NO2等)轉化為其單質除去,轉化流程如圖:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 把SO2通入紫色石蕊溶液中,石蕊溶液 會變紅 | |
| B. | 把SO2通入品紅溶液中,品紅溶液會褪色 | |
| C. | 將足量SO2通入酸性高錳酸鉀溶液中,溶液褪色 | |
| D. | 把SO2通入氯化鋇溶液中,溶液會出現白色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
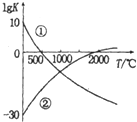 氮氣是制備含氮化合物的一種重要物質,而含氮化合物的用途廣泛,如圖表示兩個常見固氮反應的平衡常數對數值(IgK)與溫度的關系:
氮氣是制備含氮化合物的一種重要物質,而含氮化合物的用途廣泛,如圖表示兩個常見固氮反應的平衡常數對數值(IgK)與溫度的關系:| A. | 反應①和②均為放熱反應 | |
| B. | 升高溫度,反應①的反應速率減小 | |
| C. | 在常溫下,利用反應①固氮和利用反應②固氮反應程度相差很大 | |
| D. | 在1000℃時,反應①和反應②體系中N2的濃度一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在滴加酸堿指示劑酚酞試液后呈現紅色的溶液中:Na+、Cl-、AlO2-、CO32- | |
| B. | 在由水電離出的c(H+)=1×10-12mol/L的溶液中:HCO3-、Al3+、NH4+、ClO- | |
| C. | 在$\frac{c({H}^{+})}{c(0{H}^{-})}$=1×1012的溶液中:Fe2+、Mg2+、CO32-、NO3- | |
| D. | 在AlCl3溶液中:K+、NO3-、S2-、Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在電解水實驗中,加入硫酸鈉可以提高電解效率 | |
| B. | 碳酸氫鈉溶液與硫酸鋁溶液混合有沉淀和氣體生成 | |
| C. | 鐵制品在海水中比在純水中更易腐蝕 | |
| D. | 在雙氧水中加FeCl3溶液可使產生O2速率加快 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入稀鹽酸產生無色氣體,將氣體通入澄清石灰水中,溶液變渾濁,一定有CO32- | |
| B. | 加入氯化鋇溶液有白色沉淀產生,再加鹽酸,沉淀不消失,一定有SO42- | |
| C. | 加入氫氧化鈉溶液并加熱,產生的氣體能使濕潤紅色石蕊試紙變藍,一定有NH4+ | |
| D. | 某溶液中加入硝酸銀溶液,產生白色沉淀,該溶液中一定含有Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com