
2- 4 |
| O | 2- 4 |
| O | 2- 4 |
| O | 2- 4 |
| ||
| ||
| ||
| ||
| 6×58.5 |
| m |
| 2×198 |
| 198g |


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

| 實驗記錄 | 實驗分析或實驗結論 | |
| 現象 | 硬質玻璃管內物質由綠色變為紅棕色 | 說明生成的物質有 |
| 干燥管內物質顏色由白色變為 | 說明生成的物質有 | |
數據 | 稱取綠礬樣品質量11.12g | |
| C裝置增重1.28g | 說明生成SO2 | |
| A裝置中生成白色沉淀4.66g | 說明生成SO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1L 0.1 mol?L-1碳酸鈉溶液中的陰離子總數為0.1NA |
| B、將400 mL 1 mol/L的HNO3溶液與7 g Fe粉充分反應,轉移電子數為0.375NA |
| C、標準狀況下,14 g氮氣中共用電子對的數目為1.5NA |
| D、已知反應N2(g)+3H2(g)?2NH3(g)△H=-91.8KJ/mol中反應物的轉化率為30%,相同條件下,當放出91.8 kJ熱量時,生成氨分子的數目為0.6NA |
查看答案和解析>>
科目:高中化學 來源: 題型:
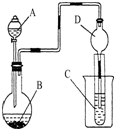
| A、若A為濃鹽酸,B為MnO2,C中盛品紅溶液,則C中溶液褪色 |
| B、若A為醋酸,B為貝殼,C中盛澄清石灰水,則C中溶液變渾濁 |
| C、實驗儀器D主要起到洗氣的作用 |
| D、若A為濃氨水,B為生石灰,C中AlCl3溶液,則C中先產生白色沉淀后沉淀又溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:
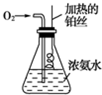 按如圖所示的裝置進行實驗:
按如圖所示的裝置進行實驗:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com