
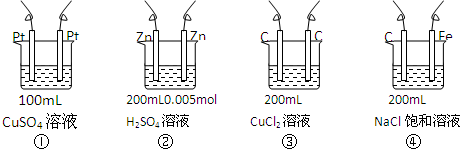
| A. | ①<②<③<④ | B. | ①<③<②<④ | C. | ②<①<④<③ | D. | ①<②<④<③ |
分析 ①中析出銅和氧氣,所以電解一段時間后,溶液中酸性增強,②中析出氫氣,所以氫離子濃度降低,根據轉移電子計算①②中氫離子濃度相對大小,比較酸性強弱,③是電解溶質本身④中陰極上析出氫氣,陽極上析出氯氣,導致溶液的堿性增強.
解答 解:①總電極反應式:2Cu2++2H2O$\frac{\underline{\;通電\;}}{\;}$2Cu+O2↑+4H+,陽極電極反應式:2H2O-4e-═4H++O2↑,通過0.002mole-,產生n(H+)=0.002mol,c(H+)=0.02mol•L-1;
②總電極反應式:Zn+2H+$\frac{\underline{\;通電\;}}{\;}$Zn2++H2↑,陰極電極反應式:2H++2e-═=H2↑,通過0.002mole-,消耗H+的物質的量為0.002mol,剩余H+的濃度:c(H$\frac{(200×1{0}^{-3}×0.005×2-0.002)}{(200×1{0}^{-3})mol•{L}^{-1}}$=0,說明H2SO4完全反應,溶質是ZnSO4;
③總電極反應式:Cu2++2Cl-$\frac{\underline{\;通電\;}}{\;}$Cu+Cl2↑,氯氣和水發生極少量的鹽酸和次氯酸;
④總電極反應式:2Cl-+2H2O$\frac{\underline{\;通電\;}}{\;}$Cl2↑+H2↑+2OH-,溶液顯堿性,
所以c(H+)的從大到小的順序:①③②④,pH與c(H+)相反,pH由小到大的順序①<③<②<④;
故選B.
點評 本題考查了電解池原理,明確陰陽極上放電的離子是解本題的關鍵,難度不大,側重于考查學生的分析能力和計算能力.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
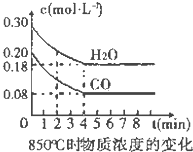 在一體積為10L的容器中,通入一定量的CO和H2O,在850℃時發生如下反應:
在一體積為10L的容器中,通入一定量的CO和H2O,在850℃時發生如下反應:| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過渡元素均為金屬元素 | |
| B. | IA族統稱為堿金屬,最外層有兩個電子的原子一定在IIA 族 | |
| C. | 含離子鍵的晶體一定是離子晶體,含共價鍵的晶體一定是分子晶體 | |
| D. | 兩種微粒,若核外電子排布完全相同,則其化學性質一定相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 病人輸液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其標簽上的部分內容如圖所示.利用標簽所提供的信息,回答下列問題:
病人輸液用的葡萄糖注射液是葡萄糖(C6H12O6)的水溶液,其標簽上的部分內容如圖所示.利用標簽所提供的信息,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:多選題
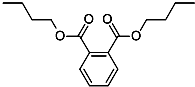 今年白酒行業塑化劑風波成為人們關注的焦點,塑化劑的其中一種鄰苯二甲酸二丁酯(DBP)的結構如圖所示,可由鄰苯二甲酸(
今年白酒行業塑化劑風波成為人們關注的焦點,塑化劑的其中一種鄰苯二甲酸二丁酯(DBP)的結構如圖所示,可由鄰苯二甲酸(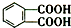 )與正丁醇發生酯化反應制得,下列有關說法不正確的是( )
)與正丁醇發生酯化反應制得,下列有關說法不正確的是( )| A. | 鄰苯二甲酸二丁酯(DBP)分子式為:C16H22O4 | |
| B. | 鄰苯二甲酸二丁酯(DBP)苯環上的一氯代物有4種 | |
| C. | 鄰苯二甲酸二丁酯(DBP)屬于乙酸乙酯的同系物 | |
| D. | 丁醇有4種不同結構,所以戊醛也有4種不同結構 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 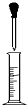 用量筒量取一定量液體時,先從試劑瓶中直接倒入大部分試劑于量筒中,至接近刻度時改用如圖所示操作,逐滴加入至刻度 用量筒量取一定量液體時,先從試劑瓶中直接倒入大部分試劑于量筒中,至接近刻度時改用如圖所示操作,逐滴加入至刻度 | |
| B. | 金屬鎂因保存不當造成失火可用細沙蓋滅,不能用泡沫滅火器 | |
| C. | 探究溫度對化學反應速率影響時,先將硫代硫酸鈉與硫酸兩種溶液混合后再用水浴加熱 | |
| D. | 熱化學方程式中,如果沒有注明溫度和壓強,表示反應熱是在25℃,101KPa測得的 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
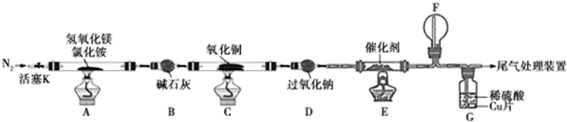
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取裝置C中反應后的少許固體于試管中 | \ |
| 步驟2:向試管中加入2mol/LH2SO4溶液 | 液中出現藍色,說明紅色固體中含有Cu2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com