
| A. | 原子半徑:W>Z>Y>X | B. | 氣態氫化物的穩定性:X<Z | ||
| C. | 最外層電子數:Y>W | D. | Y、z的氧化物都是兩性氧化物 |
分析 X、Y、Z、W為周期表中前20號元素中的四種,原子序數依次增大,W、Y為金屬元素,X原子的最外層電子數是次外層電子數的3倍,原子只能有2個電子層,最外層電子數為6,故X為O元素;Z單質是一種良好的半導體,則Z為Si;W、Y為金屬元素,W原子序數大于Si,故W處于第四周期,Y、Z原子的最外層電子數之和與X、W原子的最外層電子數之和相等,由于X處于IIA族,Y原子最外層電子數為4,Y、Z不可能同周期,則X處于IA族,Y處于ⅢA族,可推知W為K、Y為Al,據此解答.
解答 解:X、Y、Z、W為周期表中前20號元素中的四種,原子序數依次增大,W、Y為金屬元素,X原子的最外層電子數是次外層電子數的3倍,原子只能有2個電子層,最外層電子數為6,故X為O元素;Z單質是一種良好的半導體,則Z為Si;W、Y為金屬元素,W原子序數大于Si,故W處于第四周期,Y、Z原子的最外層電子數之和與X、W原子的最外層電子數之和相等,由于X處于IIA族,Y原子最外層電子數為4,Y、Z不可能同周期,則X處于IA族,Y處于ⅢA族,可推知W為K、Y為Al.
A.同周期自左而右原子半徑減小,同主族自上而下原子半徑增大,故原子半徑:K>Al>Si>O,故A錯誤;
B.非金屬性O>Si,氫化物穩定性與元素非金屬性一致,故氧元素氫化物較穩定,故B錯誤;
C.Y為Al,原子最外層電子數為3,W為K,原子最外層電子數為1,故最外層電子數:Y>W,故C正確;
D.Y、Z的氧化物分別為氧化鋁、二氧化硅,氧化鋁是兩性氧化物,二氧化硅屬于酸性氧化物,故D錯誤,
故選:C.
點評 本題考查結構性質位置關系綜合應用,推斷元素是解題關鍵,側重考查學生的分析推理能力及元素周期律.


科目:高中化學 來源: 題型:解答題
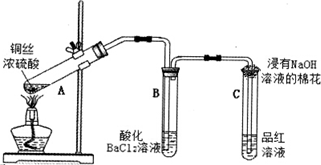
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 該氨水顯弱堿性 | |
| B. | 加水稀釋過程中,c(H+)/c(OH-)的值減小 | |
| C. | 與同溫下pH=11的NaOH溶液相比,NaOH溶液中c(Na+)大于氨水中c(NH4+) | |
| D. | 加入少量NH4Cl 固體,溶液中水的電離平衡:H2O?H++OH-向右移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
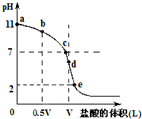 常溫時向濃度為0.1mol/L體積為VL的氨水中逐滴加入一定濃度的鹽酸,用pH計測得溶液的pH隨鹽酸的加入量而降低的滴定曲線,d點兩種溶液恰好完全反應.根據圖象回答下列問題:
常溫時向濃度為0.1mol/L體積為VL的氨水中逐滴加入一定濃度的鹽酸,用pH計測得溶液的pH隨鹽酸的加入量而降低的滴定曲線,d點兩種溶液恰好完全反應.根據圖象回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.05 mol•L-1H2CrO4溶液的pH=1 | |
| B. | 向100 mL0.l mol•L-1 H2CrO4溶液中滴入幾滴NaOH溶液,溶液中$\frac{c(Cr{O}_{4}^{2-})}{c(HCr{O}_{4}^{-})}$變大 | |
| C. | Na2CrO4溶液中:c(Na+)+c(H+)=c(CrO42-)+c(HCrO4-)+c(OH-) | |
| D. | 等濃度的:NaHCrO4溶液與NaHCO3溶液中,水的電離程度前者大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 3種 | C. | 4種 | D. | 5種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
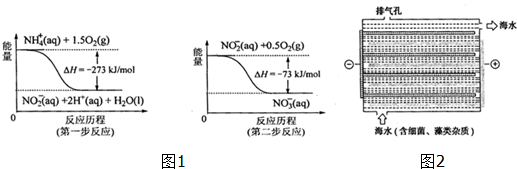
| 離子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 濃度(mol/L) | 3×10-6 | 7×10-6 | 2×10-5 | 3×10-5 | 5×10-5 | 2×10-5 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 0.1mol•L-1CH3COOH與0.1mol•L-1氨水等體積混合(PH=7):c(NH4+)=c(CH3COO-)=c(H+)=c(OH-) | |
| B. | 0.1mol•L-1HCl溶液與0.2mol•L-1氨水等體積混合(PH>7):c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-) | |
| C. | 0.1mol•L-1CH3COONa與0.1mol•L-1CaCl2溶液等體積混合:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| D. | 0.1mol•L-1Na2CO3溶液與0.1mol•L-1 NaHCO3溶液等體積混合:c(HCO3-)>0.05mol•L-1>c(CO32-)>c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com