

分析 A和濃鹽酸在加熱條件下反應生成黃綠色氣體D,則D為Cl2,A應為MnO2,生成的E為MnCl2溶液,MnO2和KOH與氧氣在熔融狀態下反應生成K2MnO4和H2O,K2MnO4在酸性條件下自身發生氧化還原反應生成KMnO4和MnO2,則B為K2MnO4,C為KMnO4,KMnO4不穩定,加熱生成K2MnO4、MnO2和O2,則F為O2,以此解答該題.
解答 解:A和濃鹽酸在加熱條件下反應生成黃綠色氣體D,則D為Cl2,A應為MnO2,生成的E為MnCl2溶液,MnO2和KOH與氧氣在熔融狀態下反應生成K2MnO4和H2O,K2MnO4在酸性條件下自身發生氧化還原反應生成KMnO4和MnO2,則B為K2MnO4,C為KMnO4,KMnO4不穩定,加熱生成K2MnO4、MnO2和O2,則F為O2,
(1)C為KMnO4,KMnO4不穩定,加熱生成K2MnO4、MnO2和O2,反應的方程式為2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
A為MnO2,可與氧氣在堿性條件下反應生成錳酸鉀,方程式為2MnO2+4KOH+O2$\frac{\underline{\;\;△\;\;}}{\;}$2K2MnO4+2H2O,
故答案為:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;2MnO2+4KOH+O2$\frac{\underline{\;\;△\;\;}}{\;}$2K2MnO4+2H2O;
(2)MnO2和濃鹽酸在加熱條件下反應生成黃綠色氣體Cl2和MnCl2溶液,反應的離子方程式為MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
K2MnO4在酸性條件下自身發生氧化還原反應生成KMnO4和MnO2,反應的離子方程式為3MnO4-+4H+=2MnO4-+MnO2↓+2H2O,
故答案為:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;3MnO42-+4H+=2MnO4-+MnO2↓+2H2O.
點評 本題考查無機物的推斷和氯氣的性質,為高頻考點,側重學生的分析能力和元素化合物知識的綜合理解和運用的考查,題目難度中等,本題注意把握KMnO4、K2MnO4、MnO2等物質的性質.


 快樂暑假暑假能力自測中西書局系列答案
快樂暑假暑假能力自測中西書局系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
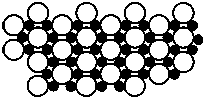 2001年3月發現硼化鎂在39K時呈超導性,可 能是人類對超導認識的新里程碑.在硼化鎂晶體的理想模型中,鎂原子和硼原子是分層排布的,一層鎂一層硼的相間排列,如圖是該晶體微觀空間中取出的部分原子沿Z軸方向的投影,白球是鎂原子投影,黑球是硼原子投影,圖中的硼原子和鎂原子投影在同一平面上.根據下圖確定硼化鎂的化學式為( )
2001年3月發現硼化鎂在39K時呈超導性,可 能是人類對超導認識的新里程碑.在硼化鎂晶體的理想模型中,鎂原子和硼原子是分層排布的,一層鎂一層硼的相間排列,如圖是該晶體微觀空間中取出的部分原子沿Z軸方向的投影,白球是鎂原子投影,黑球是硼原子投影,圖中的硼原子和鎂原子投影在同一平面上.根據下圖確定硼化鎂的化學式為( )| A. | MgB | B. | MgB2 | C. | Mg2B | D. | MgB6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 原子半徑:Y>Z>X | |
| B. | 若Y的氧化物為兩性氧化物,則Z的一種單質在空氣中易自燃 | |
| C. | 若X的氣態氫化物與Z的最高價氧化物的水化物能反應,則生成的鹽僅有一種 | |
| D. | 若Y與Z的核電荷數之和為X的4倍,則X、Y、Z的氫化物分子的立體構型分別為:V形,三角錐形,直線形 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
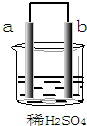
| A. | b極上發生了還原反應 | |
| B. | a是正極,b是負極 | |
| C. | a極上放出氣體,溶液的pH增大 | |
| D. | 導線中有電子流動,電子從b極流到a極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Q1+3Q2>6Q3 | B. | Q1+3Q2<6Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2=Q3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸性:HClO4>HBrO4>HIO4 | B. | P、S、C1元素最高正價依次升高 | ||
| C. | 穩定性:PH3>H2S>HCl | D. | 離子半徑:Mg2+<Na+<F- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電能轉化為化學能 | B. | 電解質溶液是稀硫酸 | ||
| C. | 電子通過外電路從正極流向負極 | D. | Zn做負極被氧化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com