
【題目】麻黃素是中樞神經興奮劑,其合成路線如圖所示。NBS是一種選擇性溴代試劑。
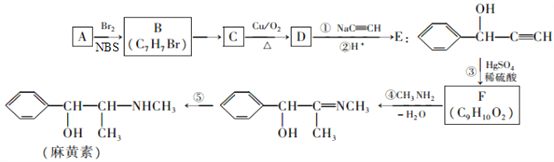
已知:①A的分子量為92
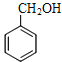
②
(1)其中A為烴,則A的分子式是__________
(2)寫出B![]() C的化學方程式_______
C的化學方程式_______
(3)實驗室檢驗D中官能團的方法為________。
(4)反應①的反應類型是______,F的結構簡式是__________。
(5)有機物N與F互為同分異構體,滿足下列條件的有機物N的結構有_____種;
①苯環上只有一個取代基 ②能發生水解反應 ③含有甲基
(6)參照上述合成路線信息,設計一條以乙醇為原料選用必要的試劑合成CH3CHOHCOCH3的流程。_____________
【答案】 C7H8 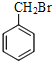 +NaOH
+NaOH![]()
 +NaBr 取物質D的樣品少量于試管中,加入銀氨溶液,水浴加熱后若有光亮的銀鏡出現說明D中含有醛基。(或加入新制取的氫氧化銅的堿性懸濁液加熱后出現紅色沉淀) 加成反應
+NaBr 取物質D的樣品少量于試管中,加入銀氨溶液,水浴加熱后若有光亮的銀鏡出現說明D中含有醛基。(或加入新制取的氫氧化銅的堿性懸濁液加熱后出現紅色沉淀) 加成反應 ![]() 5 CH3CH2OH
5 CH3CH2OH![]() CH3CHO
CH3CHO![]()
![]()
![]()
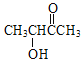
【解析】試題分析:本題考查有機推斷和有機合成,側重考查有機物分子式的確定、官能團的識別、有機物結構簡式和方程式的書寫、官能團的檢驗、限定條件同分異構體數目的確定、有機合成路線的設計。
(1)A為烴,A的相對分子質量為92,用“商余法”,92![]() 12=7……8,A的分子為C7H8。
12=7……8,A的分子為C7H8。
(2)根據流程對比A和B的分子式,A→B為取代反應;C與Cu/O2、加熱轉化為D,C→D為醇的催化氧化,C中含醇羥基,D中含醛基;D與①NaC![]() CH、②H+作用后得到E,根據E的結構簡式可逆推出D的結構簡式為
CH、②H+作用后得到E,根據E的結構簡式可逆推出D的結構簡式為![]() ,C的結構簡式為
,C的結構簡式為 ,B的結構簡式為
,B的結構簡式為 ,A的結構簡式為
,A的結構簡式為![]() 。B→C的化學方程式為
。B→C的化學方程式為 +NaOH
+NaOH![]()
 +NaBr。
+NaBr。
(3)D的結構簡式為![]() ,D中的官能團為-CHO,檢驗-CHO可用銀氨溶液或新制Cu(OH)2懸濁液,檢驗D中官能團的方法:取物質D的樣品少量于試管中,加入銀氨溶液,水浴加熱后若有光亮的銀鏡出現說明D中含有醛基。(或加入新制取的Cu(OH)2的堿性懸濁液加熱后若出現紅色沉淀說明D中含有醛基)
,D中的官能團為-CHO,檢驗-CHO可用銀氨溶液或新制Cu(OH)2懸濁液,檢驗D中官能團的方法:取物質D的樣品少量于試管中,加入銀氨溶液,水浴加熱后若有光亮的銀鏡出現說明D中含有醛基。(或加入新制取的Cu(OH)2的堿性懸濁液加熱后若出現紅色沉淀說明D中含有醛基)
(4)根據D和E的結構簡式,以及D→E的反應試劑,反應①的反應類型為加成反應。根據E→F的反應條件,E→F發生題給已知②的反應,結合F的分子式(C9H10O2),F的結構簡式為![]() 。
。
(5)F的不飽和度為5,F的同分異構體N能發生水解反應,N中含酯基,N的苯環上只有一個取代基且含有甲基;符合條件的N的結構簡式為:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,符合條件的N的結構有5種。
,符合條件的N的結構有5種。
(6)CH3CHOHCOCH3與F中含有相同的官能團,對比CH3CH2OH和CH3CHOHCOCH3的結構簡式,本題的合成路線應仿流程中C→D→E→F,CH3CH2OH先發生催化氧化反應生成CH3CHO,CH3CHO與①NaC![]() CH、②H+作用得到
CH、②H+作用得到![]() ,
,![]() 在HgSO4、稀硫酸存在下生成CH3CHOHCOCH3,合成路線為:CH3CH2OH
在HgSO4、稀硫酸存在下生成CH3CHOHCOCH3,合成路線為:CH3CH2OH![]() CH3CHO
CH3CHO![]()
![]()
![]()
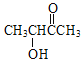 。
。


科目:高中化學 來源: 題型:
【題目】有一包白色粉末,由BaCl2、K2SO4、CaCO3、NaOH、CuSO4中的一種或幾種組成,為了探究它的成份,進行了如下實驗:下列判斷正確的是
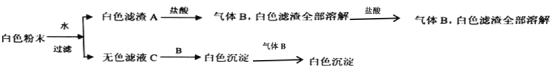
A. K2SO4、CuSO4一定不存在
B. BaCl2一定不存在
C. K2SO4、CaCO3、BaCl2一定存在
D. 濾液C中只含有BaCl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉑(Pt)可以和很多化合物形成配合物,生產生活中有重要的用途。
(1)鉑和氨水可以形成配合物。可用于提取鉑。氨水中各元素的第一電離能由大到小的順序___。
(2)二氯二吡啶合鉑是由Pt2+、Cl-和吡啶結合形成的鉑配合物,有順式和反式兩種同分異構體,科學研究表明,反式分子和順式分子一樣具有抗癌活性。
①C1-的核外電子排布式為_______。
②吡啶分子是大體積平面配體,其結構簡式為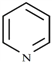 ,吡啶分子中氮原子的軌道雜化方式是_____,分子中的大π鍵可用符號
,吡啶分子中氮原子的軌道雜化方式是_____,分子中的大π鍵可用符號![]() 表示,其中m代表參與形成大π鍵的原子數,n代表參與形成大π鍵的電子數,則吡啶中的大π鍵應表示為_____;1mol吡啶中含有σ鍵的數目為________
表示,其中m代表參與形成大π鍵的原子數,n代表參與形成大π鍵的電子數,則吡啶中的大π鍵應表示為_____;1mol吡啶中含有σ鍵的數目為________
③二氯二吡啶合鉑分子中存在的微粒間作用力有_____(填字母)。
a.離子健 b.配位鍵c.金屬鍵 d.非極性鍵e.氫鍵f.極性鍵
④二氯二吡啶合鉑分子中,Pt2+的配位數是4,但是其軌道雜化方式并不是sp3。簡述理由_____________。
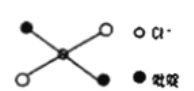
⑤反式二氯二吡啶合鉑分子結構如圖所示,該分子是_____分子(其“極性”或“非極性”)。
(3)富勒烯C60能夠與Pt結合形成一系列絡合物。富勒烯(C60)的結構如圖所示,C60屬于____晶體;C60分子中五元環與六元環的數目比為__________。
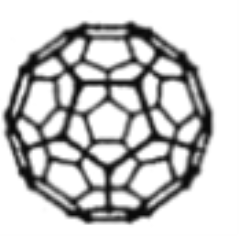
(已知簡單多面體的頂點數V、棱數E及面數F間有如下關系:V-E+F=2)。
(4)金屬鉑立方晶胞的二維投影圖如圖所示。若金屬鉑的密度dg/cm3,則晶胞參數a=___nm(列出計算式即可)。
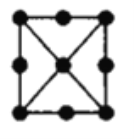
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制100mL1.0mol·L-1的NaOH溶液,下列情況不會影響溶液濃度的是
A. 容量瓶使用前有蒸餾水
B. 配制過程中,未用蒸餾水洗滌燒杯和玻璃棒
C. 俯視確定凹液面與刻度線相切
D. 稱量NaOH固體時使用了稱量紙
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳及其化合物在有機合成、能源開發等工農業方面具有十分廣泛的應用。
I.工業生產精細化工產品乙二醛(OHC-CHO)
(1)乙醇(CH3CH2OH)液相硝酸氧化法:在Cu(NO3)2催化下,用稀硝酸氧化乙醇制取乙二醛,此反應的化學方程式為_______________。該法具有原料易得、反應條件溫和等優點,但也存在比較明顯的缺點____________。
(2)乙二醇(HOCH2CH2OH)氣相氧化法
已知:2H2(g)+O2(g) ![]() 2H2O(g)ΔH=-484kJ/mol,化學平衡常數為K1
2H2O(g)ΔH=-484kJ/mol,化學平衡常數為K1
OHC-CHO(g)+2H2(g) ![]() HOCH2CH2OH(g) ΔH=-78kJ/mol,化學平衡常數為K2
HOCH2CH2OH(g) ΔH=-78kJ/mol,化學平衡常數為K2
則乙二醇氣相氧化反應HOCH2CH2OH(g)+O2(g) ![]() OHC-CHO(g)+2H2O(g)的ΔH=______;相同溫度下,該反應的化學平衡常數K=______(用含K1、K2的代數式表示)。
OHC-CHO(g)+2H2O(g)的ΔH=______;相同溫度下,該反應的化學平衡常數K=______(用含K1、K2的代數式表示)。
Ⅱ.CO2的綜合利用
(3)一定量的CO2與足量的碳在體積可變的恒壓密閉容器中發生反應C(s)+CO2(g)![]() 2CO(g)。平衡時,體系中氣體體積分數與溫度的關系如下圖所示,則下列說法正確的是______(填字母)。
2CO(g)。平衡時,體系中氣體體積分數與溫度的關系如下圖所示,則下列說法正確的是______(填字母)。
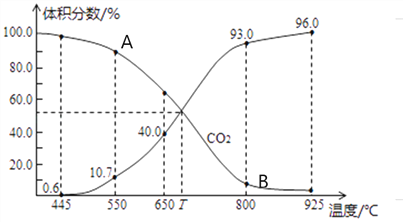
a.反應達平衡狀態時,混合氣體的平均相對分子質量保持不變
b.A點的正反應速率比B點正反應速率小
C.550℃時,若充入氦氣,則V正、V逆均減小,平衡不移動
d.T℃時,反應達平衡后CO2的轉化率為66.7%
e. T℃時,若再充入1molCO2和1molCO,平衡不移動
(4)氨氣、CO2在一定條件下可合成尿素,其反應為2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g),右圖表示合成塔中氨碳比a與CO2轉化率ω的關系。a為{n(NH3)/n(CO2)},b為水碳比{n(H2O)/n(CO2)}。則
CO(NH2)2(s)+H2O(g),右圖表示合成塔中氨碳比a與CO2轉化率ω的關系。a為{n(NH3)/n(CO2)},b為水碳比{n(H2O)/n(CO2)}。則
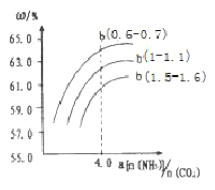
①b應控制在______
a.1.5-1.6b.1-1.1c.0.6-0.7
②a應控制在4.0的理由是_________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,取0.1mol/L的NaA和NaB兩種鹽溶液各1L,分別通入0.02molCO2,發生如下反應:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB的1L溶液分別加水稀釋至體積為VL時可能有如圖曲線,則下列說法正確的是
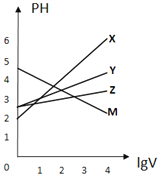
A. 相同條件下,對于c(R-)/[c(HR)·c(OH-)]的值(R代表A或B),一定存在HA>HB
B. 常溫下pH:NaA溶液>NaB溶液
C. X是HA,M是HB
D. 若常溫下濃度均為0.1mol/L的NaA和HA的溶液等體積混合,則c(A-)+c(HA)=0.2mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是由短周期元素組成的一些單質及其化合物之間的轉化關系圖。常溫常壓下,D、F、K均為無色無刺激性氣味的氣體,B是最常見的無色液體,A是由單質C在D中燃燒生成的淡黃色固體。(反應中生成的部分物質已略去)

請回答下列問題:
(1)物質A的化學式為________;
(2)化合物I的化學式為________;
(3)反應①的化學方程式為_____________;反應②的化學方程式為______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com