
 下表為某市售鹽酸試劑瓶標簽上的部分信息:
下表為某市售鹽酸試劑瓶標簽上的部分信息:分析 (1)根據物質的量濃度c=$\frac{1000ρω}{M}$計算出該鹽酸的物質的量濃度;
(2)稀釋過程中溶質的物質的量不變,據此計算出稀釋后溶液中鹽酸的濃度;
(3)根據H元素質量守恒計算出生成氫氣的物質的量,再根據V=nVm計算出生成氫氣的體積.
解答 解:(1)該鹽酸的物質的量濃度為:c=$\frac{1000ρω}{M}$=$\frac{1000×1.18×36.5%}{36.5}$mol/L=11.8mol/L,
故答案為:11.8mol/L;
(2)取該鹽酸50mL加水稀釋到500mL,稀釋過程中氯化氫的物質的量不變,則稀釋后溶液中c(HCl)=$\frac{11.8mol/L×0.05L}{0.5L}$=1.18mol/L,
故答案為:1.18mol/L;
(3)500mL稀釋后的溶液中含有HCl的物質的量為:1.18mol/L×0.5L=0.59mol,根據氫元素守恒可知生成氫氣的物質的量為:$\frac{1}{2}$×0.059mol=0.295mol,
則生成的氫氣在標況下的體積為:22.4L/mol×0.295mol=6.608L,
故答案為:6.608L.
點評 本題考查了物質的量濃度的計算、化學反應的計算,題目難度中等,注意掌握物質的量濃度的概念及計算方法,明確質量守恒定律在化學計算中的應用方法.


科目:高中化學 來源: 題型:選擇題
| A. | 用量筒量取所需濃硫酸時,仰視刻度線 | |
| B. | 將量筒中的濃硫酸倒入燒杯后,沒有用水沖洗量筒2-3次并轉移至燒杯中 | |
| C. | 用膠頭滴管滴加蒸餾水定容時,仰視刻度線 | |
| D. | 定容搖勻后,液面下降,沒有重新加蒸餾水至刻度線 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.265mol•L-1 | B. | 0.525mol•L-1 | C. | 0.21mol•L-1 | D. | 0.42mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
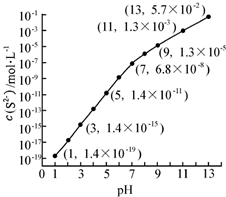 (1)25℃,在0.10mol•L-1H2S溶液中,通入HCl氣體或加入NaOH固體以調節溶液pH,溶液pH與c(S2-)關系如圖(忽略溶液體積的變化、H2S的揮發).
(1)25℃,在0.10mol•L-1H2S溶液中,通入HCl氣體或加入NaOH固體以調節溶液pH,溶液pH與c(S2-)關系如圖(忽略溶液體積的變化、H2S的揮發).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al3+、Cl-、Ca2+ | B. | Mg2+、SO42-、OH- | C. | Na+、SO32-、H+ | D. | H+、K+、OH- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com