
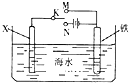
| A. | 若X為碳棒,開關K置于N處,可以加快鐵的腐蝕 | |
| B. | 若X為碳棒,開關K置于N處,則X極附近溶液變黃色 | |
| C. | 若X為鋅,開關K置于M處,保護鐵電極則為犧牲陽極的陰極保護法 | |
| D. | 若X為鋅,開關K置于M處,則X電極的反應式為:O2+4e+2H2O→4OH- |
分析 A.若X為碳棒,開關K置于N處,此時構成的是電解池;
B.若X為碳棒,開關K置于N處,此時構成的是電解池,陽極上氯離子失電子;
C.若X為鋅,開關K置于M處,此時構成的是原電池,X為負極,Y為正極;
D.若X為鋅,開關K置于M處,為鋅的吸氧腐蝕.
解答 解:A.若X為碳棒,開關K置于N處,此時構成的是電解池,鐵棒做陰極,陰極上陽離子發生還原反應,Fe不反應,故可以減緩鐵的腐蝕,故A錯誤;
B.若X為碳,開關K置于N處,此時構成的是電解池,X為陽極,陽極上陰離子失電子生成氯氣,因此X極上會有黃綠色氣體生成,溶液不能變黃色,故B錯誤;
C.若X為鋅,開關K置于M處,此時構成的是原電池,X為負極,Y為正極,Fe作正極被保護,即保護鐵電極則為犧牲陽極的陰極保護法,故C正確;
D.若X為鋅,開關K置于M處,為鋅的吸氧腐蝕,X上Zn失電子生成鋅離子,則X電極的反應式為:Zn-2e=Zn2+,故D錯誤.
故選C.
點評 本題綜合考查了電解池、原電池的內容,屬于中等難度題型,解題時,應首先判斷所給的裝置是原電池還是電解池,其次再根據確定的裝置類型進行解答.


科目:高中化學 來源: 題型:解答題
 (1)實驗室用NaNO3固體配制500mL 0.40mol/L NaNO3溶液.
(1)實驗室用NaNO3固體配制500mL 0.40mol/L NaNO3溶液.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Kw>1×10-14 | B. | 水電離的c(H+)>1×10-13 mol/L | ||
| C. | pH>13 | D. | c(OH-)=c(H+)+c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol 任何物質所含的分子數均為NA | |
| B. | 14 g氮氣所含的氮原子數為NA | |
| C. | 標準狀況下,22.4 L水所含的水分子數為NA | |
| D. | 在鈉與氯氣的反應中,1 mol鈉失去電子的數目為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a=b | B. | HA與BOH的電離常數相等 | ||
| C. | 混合溶液中,c(H+)=$\sqrt{{K}_{W}}$mol/L | D. | 混合溶液中,c(H+)+c(B+)═c(OH-)+c(A-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯酚與碳酸氫鈉溶液混合:C6H5OH+HCO3-→C6H5O-+CO2↑+H2O | |
| B. | 向FeBr2溶液中通入等量Cl2:2Fe2++2Br-+2Cl2→2Fe3++Br2+4Cl- | |
| C. | 將Al投入NaOH的重水溶液:2Al+2OH-+2D2O→2AlO2-+3D2↑ | |
| D. | Ca(HCO3)2溶液中加入足量的Ba(OH)2溶液:Ca2++2HCO3-+2OH-→CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
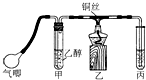 利用如圖裝置進行乙醇的催化氧化實驗并制取乙醛(試管丙中用水吸收產物).
利用如圖裝置進行乙醇的催化氧化實驗并制取乙醛(試管丙中用水吸收產物).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室制備乙烯時,產生的氣體使溴水褪色,能證明有乙烯生成 | |
| B. | 除去溴苯中的溴,可用稀NaOH溶液反復洗滌,并用分液漏斗分液 | |
| C. | 加熱NaOH和少量溴乙烷的混合液后滴加硝酸銀,可生成淺黃色沉淀 | |
| D. | 制取硝基苯時,試管中先加入濃H2SO4,再逐滴滴入濃HNO3和苯,振蕩混合均勻后,保持55℃水浴加熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
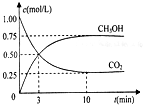 CO2和CH4是兩種重要的溫室氣體,通過CH4和CO2反應制造更高價值化學品是目前的研究目標.
CO2和CH4是兩種重要的溫室氣體,通過CH4和CO2反應制造更高價值化學品是目前的研究目標.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com