
【題目】下列與有機物的結(jié)構(gòu)、性質(zhì)的有關(guān)敘述中正確的是( )
A.等物質(zhì)的量的乙烯與乙醇完全燃燒消耗氧氣的物質(zhì)的量相等
B.乙烯、氯乙烯、聚乙烯均可使酸性高錳酸鉀溶液褪色
C.分餾、干餾都是物理變化,裂化、裂解都是化學(xué)變化
D.苯乙烯和甲苯分子內(nèi)所有原子可能共平面
【答案】A
【解析】
A.完全燃燒時,1mol乙烯(C2H4)消耗3molO2,1mol乙醇(C2H6O)消耗3molO2,兩者消耗O2物質(zhì)的量相等,A正確;
B.乙烯、氯乙烯均含碳碳雙鍵,而聚乙烯不含雙鍵,則只有乙烯、氯乙烯可使酸性高錳酸鉀溶液褪色, B錯誤;
C.分餾根據(jù)石油中各成分沸點的不同將其分離開,是物理變化,干餾是將煤隔絕空氣加強熱,既有物理變化又有化學(xué)變化,裂化、裂解都是化學(xué)變化, C錯誤;
D.苯乙烯(![]() )由于苯環(huán)和碳碳雙鍵的存在,所有原子可以共平面,甲苯(
)由于苯環(huán)和碳碳雙鍵的存在,所有原子可以共平面,甲苯(![]() )1號位置的甲基C是sp3雜化,空間構(gòu)型為四面體形,不可能所有原子共平面,D錯誤;
)1號位置的甲基C是sp3雜化,空間構(gòu)型為四面體形,不可能所有原子共平面,D錯誤;
故選A。


科目:高中化學(xué) 來源: 題型:
【題目】下列是某興趣小組根據(jù)教材實驗設(shè)計的一個能說明碳酸鈉與碳酸氫鈉熱穩(wěn)定性的套管實驗。請觀察如下圖所示實驗裝置,分析實驗原理,并判斷下列說法和做法,其中不科學(xué)的是( )

A. 甲為小蘇打,乙為純堿
B. 要證明碳酸氫鈉受熱能產(chǎn)生水,可在小試管內(nèi)塞上沾有無水硫酸銅粉末的棉花球
C. 加熱不久就能看到A燒杯的澄清石灰水變渾濁
D. 整個實驗過程中都沒有發(fā)現(xiàn)A燒杯的澄清石灰水變渾濁
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】已知NA是阿伏加德羅常數(shù)的值,下列說法錯誤的是( )
A.3 g 3He含有的中子數(shù)為1NA
B.1 L 0.1 mol·L1磷酸鈉溶液含有的![]() 數(shù)目為0.1NA
數(shù)目為0.1NA
C.1 mol K2Cr2O7被還原為Cr3+轉(zhuǎn)移的電子數(shù)為6NA
D.常溫下,11g CO2所含的共用電子對數(shù)目為NA
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】已知某化合物的晶體是由如圖所示的最小結(jié)構(gòu)單元密置堆積而成,下列關(guān)于該化合物敘述錯誤的是( )
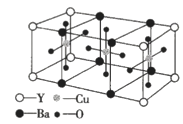
A.該化合物的化學(xué)式是YBa2Cu3O6
B.1mol該化合物中含有1molY
C.1mol該化合物中含有3molCu
D.1mol該化合物中含有2molBa
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】A、B是兩種有刺激氣味的氣體。試根據(jù)下列實驗事實填空。
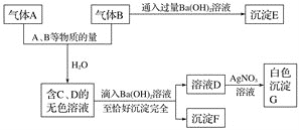
(1)寫出A~F各物質(zhì)的化學(xué)式:
A__________、B__________、C__________、D__________、E__________、F__________。
(2)寫出A、B跟水反應(yīng)的離子方程式:______________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】科學(xué)家合成了一種新化合物(如圖所示),其中X、Y是第三周期的非金屬元素,各原子均滿足8電子穩(wěn)定結(jié)構(gòu)。
完成下列填空:

(1)硅原子最外電子層有________種運動狀態(tài)不同的電子,占據(jù)______個軌道。
(2)由題意可推知Y是Cl,推得此結(jié)論的依據(jù)是__________________。X和Si之間共用電子對偏離________。
(3)SiCl4和CCl4分子空間結(jié)構(gòu)相同,則SiCl4中鍵角是_________。請說明SiCl4和CCl4沸點高低的理由。__________________________________________。
(4)黃磷(P4)與過量濃NaOH溶液反應(yīng),產(chǎn)生PH3和次磷酸鈉(NaH2PO2),補全并配平該反應(yīng)的化學(xué)方程式,標(biāo)出電子轉(zhuǎn)移的數(shù)目和方向:_____P4+_____NaOH+_________→_____PH3↑+_____NaH2PO2,____________________.其中氧化劑和還原劑質(zhì)量比為________。根據(jù)題意可判斷H3PO2是________元酸(填“一”、“二”或“三”)。
(5)已知磷酸二氫鈉(NaH2PO4)溶液呈酸性,該溶液中含磷元素的離子濃度由大到小的順序是:__________________________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】請回答下列問題:
(1)某元素X基態(tài)原子的最外層有3個未成對電子,次外層有2個電子,其價電子排布圖為___,其原子核外有___種不同運動狀態(tài)的電子;其最低價氫化物電子式為___,中心原子采用___雜化,分子立體構(gòu)型為___。
(2)某元素Y基態(tài)原子的M層全充滿,N層沒有成對電子,只有一個未成對電子,其元素名稱為___,Y+的外圍電子排布式為___,該元素固體單質(zhì)常常采用___堆積方式,配位數(shù)為___,空間利用率為___。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】某實驗小組探究AgNO3溶液與Na2SO3溶液的反應(yīng)。
實驗I | 操作 | 現(xiàn)象 |
| 滴加5滴0.1mol/L Na2SO3溶液,振蕩 | 產(chǎn)生白色沉淀,測得混合溶液pH=5 |
繼續(xù)滴加0.1mol/L Na2SO3溶液,振蕩 | 白色沉淀增多,繼續(xù)滴加,白色沉淀消失,測得混合溶液pH=9 |
資料:Ag2SO3,白色固體,難溶于水;Ag2SO4,白色固體,微溶于水;AgOH,白色固體,常溫下不穩(wěn)定,易分解產(chǎn)生棕褐色固體。
(1)測得0.1mol/L Na2SO3溶液pH=10,用離子方程式解釋原因:_______。
(2)實驗小組對白色沉淀的成分提出猜想:
①可能含Ag2SO3。
②可能含Ag2SO4,理由是________。
③可能含AgOH。
實驗產(chǎn)生的白色沉淀放置一段時間后未發(fā)生明顯變化,排除猜想③。
(3)檢驗白色沉淀的成分
(資料:Ag++2S2O32![]() Ag(S2O3)23,Ag(S2O3)23在溶液中穩(wěn)定存在。)
Ag(S2O3)23,Ag(S2O3)23在溶液中穩(wěn)定存在。)
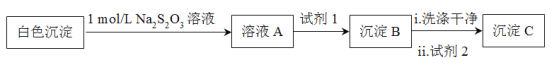
測得沉淀C質(zhì)量小于沉淀B,試劑1和試劑2分別是_____、______,說明白色沉淀是Ag2SO3和Ag2SO4的混合物。
(4)探究白色沉淀消失的原因。實驗小組設(shè)計對照實驗:
實驗II | 實驗III | |
實驗操作 |
|
|
現(xiàn)象 | 沉淀溶解 |
① 補充實驗III的實驗操作及現(xiàn)象:_______,證明SO32使白色沉淀溶解。
② 查閱資料:Ag2SO3能溶于過量Na2SO3溶液中形成Ag(SO3)23。白色沉淀中含有g2SO4,但還能全部溶解于Na2SO3溶液的原因是______。
(5)探究AgNO3溶液與Na2SO3溶液能否發(fā)生氧化還原反應(yīng)。
實驗IV | 操作 | 現(xiàn)象 |
| 步驟i:滴加一定體積0.1 mol/L Na2SO3溶液 | 產(chǎn)生白色沉淀 |
步驟ii:再加入NaOH溶液調(diào)pH=14,振蕩 | 白色沉淀變黑,經(jīng)檢驗為Ag |
步驟ii中Ag2SO3發(fā)生反應(yīng)的離子方程式是_________。
(6)綜合實驗I和IV,說明AgNO3溶液與Na2SO3溶液的反應(yīng)類型與_______有關(guān)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】某研究小組利用軟錳礦![]() 主要成分為
主要成分為![]() ,另含少量鐵,鈣,銅等金屬化合物
,另含少量鐵,鈣,銅等金屬化合物![]() 作脫硫劑,通過如下簡化流程,既脫除燃煤尾氣中的
作脫硫劑,通過如下簡化流程,既脫除燃煤尾氣中的![]() ,又制得電池材料
,又制得電池材料![]() 反應(yīng)條件已省略
反應(yīng)條件已省略![]()
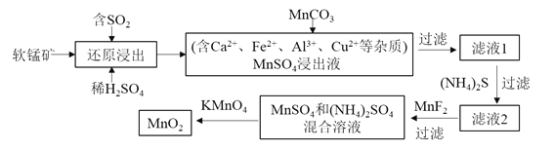
請回答下列問題:
![]() 上述還原浸出是脫硫過程,實現(xiàn)了 ______
上述還原浸出是脫硫過程,實現(xiàn)了 ______ ![]() 選填編號
選填編號![]() .
.
![]() 廢氣物的綜合利用
廢氣物的綜合利用
![]() 臭氧層空洞的減少
臭氧層空洞的減少
![]() 白色污染的減少
白色污染的減少
![]() 酸雨的減少
酸雨的減少
![]() 寫出上述軟錳礦經(jīng)還原浸出生成
寫出上述軟錳礦經(jīng)還原浸出生成![]() 的化學(xué)方程式是 ______ .
的化學(xué)方程式是 ______ .
![]() 用
用![]() 能除去還原浸出液中的
能除去還原浸出液中的![]() ,請用離子方程式解釋其原因是 ______ .
,請用離子方程式解釋其原因是 ______ .
![]() 加入
加入![]() 的目的主要是除去 ______ ;加入
的目的主要是除去 ______ ;加入![]() 的目的主要是除去 ______ ;
的目的主要是除去 ______ ;![]() 填離子符號
填離子符號![]()
![]() 下列各組試劑中,能準(zhǔn)確測定一定體積燃煤尾氣中
下列各組試劑中,能準(zhǔn)確測定一定體積燃煤尾氣中![]() 含量的是 ______
含量的是 ______ ![]() 填編號
填編號![]()
a.NaOH溶液、石蕊試液
b.稀![]() 酸化的
酸化的![]() 溶液
溶液
c.碘水、淀粉溶液
d.氨水、石蕊試液
![]() 用電化學(xué)法模擬工業(yè)處理
用電化學(xué)法模擬工業(yè)處理![]() 將硫酸工業(yè)尾氣中的
將硫酸工業(yè)尾氣中的![]() 通入如圖裝置
通入如圖裝置![]() 電均為惰性材料
電均為惰性材料![]() 進行實驗,可用于制備硫酸,同時獲得電能:
進行實驗,可用于制備硫酸,同時獲得電能:
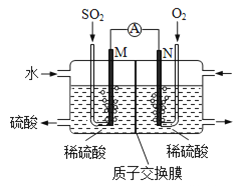
![]() 極發(fā)生的電極反應(yīng)式為 ______ .
極發(fā)生的電極反應(yīng)式為 ______ .
![]() 若使該裝置的電流強度達到
若使該裝置的電流強度達到![]() ,理論上每分鐘應(yīng)向負(fù)極通入標(biāo)準(zhǔn)狀況下氣體的體積為 ______
,理論上每分鐘應(yīng)向負(fù)極通入標(biāo)準(zhǔn)狀況下氣體的體積為 ______ ![]() 保留3位小數(shù),已知:1個
保留3位小數(shù),已知:1個![]() 所帶電量為
所帶電量為![]() .
.
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com