
【題目】已知NA是阿伏加德羅常數的值,下列說法錯誤的是( )
A.3 g 3He含有的中子數為1NA
B.1 L 0.1 mol·L1磷酸鈉溶液含有的![]() 數目為0.1NA
數目為0.1NA
C.1 mol K2Cr2O7被還原為Cr3+轉移的電子數為6NA
D.常溫下,11g CO2所含的共用電子對數目為NA
【答案】B
【解析】
A. 3He的中子數為3-2=1,則3g3He的中子數為3g÷3g/mol×NA/mol=1NA,故A正確;
B. 磷酸鈉為強堿弱酸鹽,磷酸根離子在水溶液中會發生水解,則1 L 0.1 mol·L1的磷酸鈉溶液中磷酸根離子的個數小于1 L× 0.1 mol·L1×NA =0.1NA,故B錯誤;
C. 重鉻酸鉀被還原為鉻離子時,鉻元素從+6降低到+3。1mol重鉻酸鉀中含2molCr原子,故轉移的電子數為1mol×2×3×NA/mol=6NA,故C正確;
D. 常溫下,11g CO2所含的共用電子對數目為11g÷44g/mol×4×NA /mol= NA,故 D正確;
故選:B。


科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A.中和熱測定實驗中需要的玻璃儀器有:燒杯、量筒、溫度計、環形玻璃攪拌棒
B.乙烯的燃燒熱為1411.3 kJ·mol1,則乙烯燃燒的熱化學方程式為C2H4(g)+3O2(g)![]() 2CO2(g)+2H2O(g) ΔH= 1411.3 kJ·mol1
2CO2(g)+2H2O(g) ΔH= 1411.3 kJ·mol1
C.用石墨電極電解1 L 0.1 mol·L1 CuSO4溶液,若反應產生0.1 mol O2,則向原溶液中加入0.2 mol CuO能恢復至原濃度
D.用pH試紙分別測定氯水和鹽酸的pH,比較兩溶液的酸性強弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在剛性容器中發生反應:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g),一定壓強下,平衡時H2的轉化率α(H2)隨溫度T、投料比
C2H5OH(g)+3H2O(g),一定壓強下,平衡時H2的轉化率α(H2)隨溫度T、投料比![]() 的變化關系如圖所示。下列說法錯誤的是
的變化關系如圖所示。下列說法錯誤的是
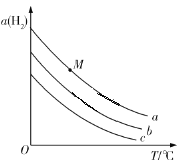
A.投料比![]() 的大小關系是:a>b>c
的大小關系是:a>b>c
B.圖中M點對應的平衡,若容積不變,充入He,則α(H2)不變
C.該反應的平衡常數K(600 ℃)>K(500 ℃)
D.若題圖表示相同投料時,不同壓強下α(H2)隨T的變化關系,則壓強最大的是a
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是第三周期部分元素的電離能數據,下列說法正確的是( )
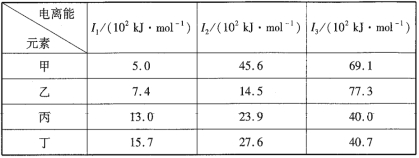
A.甲的金屬性比乙弱B.乙的最高正化合價為+1
C.丙一定為非金屬元素D.丁一定是金屬元素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用CO合成甲醇(CH3OH)的化學方程式為CO(g)+2H2(g)CH3OH(g) ΔH<0,按照相同的物質的量投料,測得CO在不同溫度下的平衡轉化率與壓強的關系如圖所示。下列說法正確的是 ( )
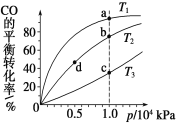
A.溫度:T1>T2>T3
B.正反應速率:v(a)>v(c) v(b)>v(d)
C.平均摩爾質量:M(a)>M(c) M(b)>M(d)
D.平衡常數:K(a)<K(c) K(b)=K(d)
查看答案和解析>>
科目:高中化學 來源: 題型:
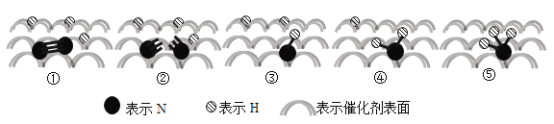
【題目】2007年諾貝爾化學獎授予埃特爾以表彰其對于合成氨反應機理的研究,氮氣和氫氣分子在催化劑表面的部分變化過程如圖所示,下列說法不正確的是( )
N2(g)+3H2(g)![]() 2NH3(g) △H = 92 kJ/mol
2NH3(g) △H = 92 kJ/mol
A.升高溫度不能提高一段時間內NH3的產率
B.圖①→②過程吸熱,圖②→③過程放熱
C.N2在反應過程中三鍵均發生斷裂
D.反應過程中存在NH、NH2等中間產物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用如圖裝置進行實驗,1小時后觀察到生鐵明顯銹蝕,由此得出的結論是
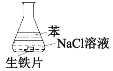
A.屬于化學腐蝕
B.O2未參與反應
C.負極反應2Fe-6e+3H2O→Fe2O3+6H+
D.正極反應O2+4e- +2H2O→4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列與有機物的結構、性質的有關敘述中正確的是( )
A.等物質的量的乙烯與乙醇完全燃燒消耗氧氣的物質的量相等
B.乙烯、氯乙烯、聚乙烯均可使酸性高錳酸鉀溶液褪色
C.分餾、干餾都是物理變化,裂化、裂解都是化學變化
D.苯乙烯和甲苯分子內所有原子可能共平面
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO2 和CH4是常見的化合物,同時也是常用的化工原料。
Ⅰ.以CO2與NH3為原料可以合成尿素[CO(NH2)2]。合成尿素的反應為2NH3(g) + CO2(g) ![]() CO(NH2)2(s) + H2O(g)。
CO(NH2)2(s) + H2O(g)。
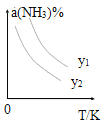
(1)在不同溫度及不同y值下合成尿素,達到平衡時,氨氣轉化率變化情況如圖所示。
①該反應的ΔH_____0(填“>” 或、“<” ),該反應自發進行的條件是_______________ (填“低溫”“高溫”或“任意溫度”) 若y表示反應開始時的氨碳比[![]() ],則y1________y2。(填“>”、“<”或“=”);
],則y1________y2。(填“>”、“<”或“=”);
(2)t℃時,若向容積固定的密閉容器中加入一定量的 NH3和CO2合成尿素,下列敘述能說明此反應達到平衡狀態的是________ (填字母)。
a.混合氣體的平均相對分子質量保持不變
b.CO2和NH3的體積分數保持不變
c.CO2和NH3的轉化率相等
d.混合氣體的密度保持不變
e.1molCO2生成的同時有 2molN—H鍵斷裂
II.工業上用CH4與水蒸氣在一定條件下制取H2,:CH4(g) + H2O(g) ![]() CO(g) + 3H2(g) ΔH = + 203 kJmol-1
CO(g) + 3H2(g) ΔH = + 203 kJmol-1
①該反應逆反應速率表達式為:v逆=kc(CO) c3(H2),k 為速率常數,在某溫度下測得實驗數據如表:
CO濃度(molL-1) | H2濃度(molL-1) | 逆反應速率(molL-1min-1) |
0.05 | c1 | 4.8 |
c2 | c1 | 19.2 |
c2 | 0.1 | 8.1 |
由上述數據可得該溫度下,該反應的逆反應速率常數k為____L3mol-3min-1。
②某溫度下,在體積為3 L的密閉容器中通入物質的量均為3 mol的CH4和水蒸氣,發生上述反應,5分鐘時達到平衡,此時H2的體積分數為60%,則在5分鐘內用CH4濃度變化表示的平均反應速率v(CH4)=________;該溫度下該反應的平衡常數K=________。平衡后再向容器中加入1 mol CH4和1 mol CO,平衡_______移動(填“正反應方向”或“逆反應方向”或“不”)。
III.在常溫下,將0.02mol CO2通入200mL 0.15mol/L的/span>NaOH溶液中,充分反應后下列關系式中正確的是_____________________
A.c(Na+)>c(HCO3-)> c(CO32-)>c(OH-)>c(H+)
B.3c (Na+)=2[c(CO32-)+ c(HCO3-)+ c(H2CO3)]
C.c (Na+)+c(H+)=c(HCO3-)+ c(CO32-)+c(OH-)
D.c(HCO3-)+ 3c(H2CO3)+2c(H+)= c(CO32-)+2c(OH-)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com