
分析 (1)加入NaOH溶液后,NaOH和H+反應導致平衡正向移動;
(2)向加入NaOH溶液的(l)中再加入過量稀H2SO4,c(H+)增大平衡逆向移動;
(3)向原溶液中加入Ba(NO3)2溶液,生成黃色沉淀BaCrO4,平衡正向移動;
(4)要使上述溶液顏色加深,應該使c(CrO42-)增大;
(5)用0.05mo1K2Cr2O7配制成1L K2CrO4溶液,其中CrO42-的濃度小于10-5mol/L.則配制時除K2Cr2O7、H2O外,還需要加入物質促進Cr2O72-水解且不能引進新的雜質,配制時需用到的玻璃儀器除燒杯、玻璃棒之外還要1000mL容量瓶、膠頭滴管.
解答 解:(1)加入NaOH溶液后,NaOH和H+反應導致c(H+)減小,平衡正向移動,溶液呈黃色,
故答案為:黃;NaOH和H+反應導致c(H+)減小,平衡正向移動;
(2)向加入NaOH溶液的(l)中再加入過量稀H2SO4,c(H+)增大平衡逆向移動,溶液呈橙色,故答案為:橙;c(H+)增大平衡逆向移動;
(3)向原溶液中加入Ba(NO3)2溶液,生成黃色沉淀BaCrO4,c(CrO42-)減小,平衡正向移動,溶液顏色變淺,故答案為:正向移動;變淺;
(4)要使上述溶液顏色加深,應該使c(CrO42-)增大,可以加入堿液、降低溫度等方法實現,
故答案為:加入堿液、降低溫度;
(5)用0.05mo1K2Cr2O7配制成1L K2CrO4溶液,其中CrO42-的濃度小于10-5mol/L.則配制時除K2Cr2O7、H2O外,還需要加入物質促進Cr2O72-水解且不能引進新的雜質,應該加入KOH溶液,配制時需用到的玻璃儀器除燒杯、玻璃棒之外還要1000mL容量瓶、膠頭滴管,1000mL容量瓶配置溶液、膠頭滴管定容,
故答案為:KOH溶液;1000mL容量瓶、膠頭滴管.
點評 本題考查外界條件對化學平衡移動影響,為高頻考點,側重考查學生分析判斷能力,加入和生成物離子的物質促進水解、加入和生成物離子相同的離子抑制水解,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 容器內壓強不隨時間變化 | B. | 化學反應速率關系是:2υ正(X)=υ正(Y) | ||
| C. | 容器內氣體密度不隨時間變化 | D. | 容器內X、Y、Z的濃度之比為l:2:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 容器編號 | 溫度(℃) | 起始物質的量(mol) | 平衡物質的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | x | |
| Ⅱ | 387 | 0.40 | y | |
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
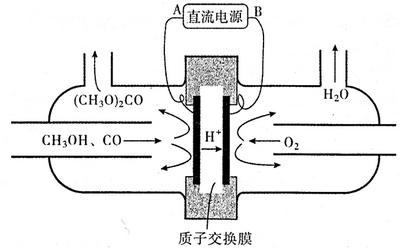
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
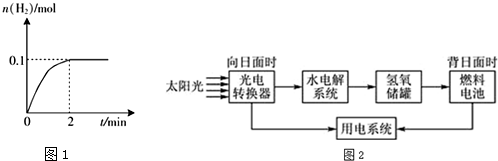
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
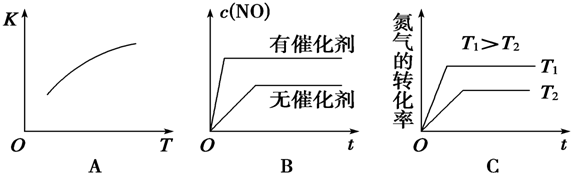
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 逆反應速率增大,正反應速率減小,平衡向逆反應方向移動 | |
| B. | 逆反應速率減小,正反應速率增大,平衡向正反應方向移動 | |
| C. | 正、逆反應速率都增大,平衡向正反應方向移動 | |
| D. | 正、逆反應速率都減小,平衡向逆反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
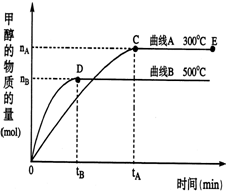 一定條件下,在體積為2L的密閉容器中,一氧化碳與氫氣在催化劑作用反應生成甲醇:CO(g)+2H2(g)?CH3OH(g).根據題意完成下列各題:
一定條件下,在體積為2L的密閉容器中,一氧化碳與氫氣在催化劑作用反應生成甲醇:CO(g)+2H2(g)?CH3OH(g).根據題意完成下列各題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol/L的(NH4)2SO4溶液:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1 mol/L的NaHCO3溶液:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 將0.2 mol/L NaA溶液和0.1 mol/L鹽酸等體積混合所得溶液:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| D. | 0.02mol/L CH3COOH溶液和0.01 mol/L NaOH溶液等體積混合所得溶液:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com