
 一定條件下2L的密閉容器中,反應aA(g)+bB(g)?cC(g)+dD(g)達到平衡.
一定條件下2L的密閉容器中,反應aA(g)+bB(g)?cC(g)+dD(g)達到平衡.分析 (1)根據V=$\frac{△c}{△t}$計算A的平均反應速率;
(2)擴大容器體積即減小壓強,反應速率減小,平衡向氣體體積增大的方向移動;
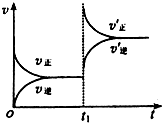
(3)根據反應速率(v)與時間(t)的關系圖,則t1時刻正逆反應速率都增大并且向正反應方向移動,據此分析.
解答 解:(1)若起始時A為l mol,反應2min達到平衡,A剩余0.4mol,則在0~2min內A的平均反應速率V=$\frac{△c}{△t}$=$\frac{\frac{1-0.4}{2}}{2}$=0.15mo1/(L•min),故答案為:0.15;
(2)擴大容器體積即減小壓強,反應速率減小,平衡向氣體體積增大的方向移動,又平衡向逆反應方向移動即為氣體體積增大的方向,所以a+b>c+d,故答案為:>;減小;
(3)根據反應速率(v)與時間(t)的關系圖,則t1時刻正逆反應速率都增大并且向正反應方向移動,又該反應為氣體體積減小的可逆反應,所以應為升壓即縮小容器體積,故選:b.
點評 本題考查化學反應速率的計算以及平衡移動的分析,題目難度不大,本題注意壓強對平衡的移動原理.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:多選題
| A. | 平衡向正反應方向移動了 | B. | 物質A的轉化率降低了 | ||
| C. | C為氣態 | D. | C為固態或液態 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2LCO和2LCO2 | B. | 標準狀況下22.4LH2O和1mol O2 | ||
| C. | 0,4克H2和4.48L HCl | D. | 18克水和標準狀況下22.4L CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 反應時間 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 0 min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | |||
| 20min | 1 | |||
| 30min | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 元素編號 | 元素性質或原子結構 |
| X | 最外層電子數是次外層電子數的2倍 |
| Y | 常溫下單質為雙原子分子,其氫化物水溶液呈堿性 |
| Z | 第三周期元素的簡單離子中半徑最小 |
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com