
| 元素編號 | 元素性質或原子結構 |
| X | 最外層電子數是次外層電子數的2倍 |
| Y | 常溫下單質為雙原子分子,其氫化物水溶液呈堿性 |
| Z | 第三周期元素的簡單離子中半徑最小 |
 .
.分析 X、Y、Z三種短周期元素,X元素原子最外電子數是次外層電子數的2倍,則X原子有2個電子層,最外層電子數為4,則X為碳元素;Y元素常溫下單質為雙原子分子,其氫化物的水溶液呈堿性,則Y為氮元素;Z為第三周期元素的簡單離子中半徑最小,則Z為Al元素,據此解答.
解答 解:X、Y、Z三種短周期元素,X元素原子最外電子數是次外層電子數的2倍,則X原子有2個電子層,最外層電子數為4,則X為碳元素;Y元素常溫下單質為雙原子分子,其氫化物的水溶液呈堿性,則Y為氮元素;Z為第三周期元素的簡單離子中半徑最小,則Z為Al元素,
(1)碳元素的一種同位素可測定文物年代,這種同位素的符號是614C,鋁離子的結構示意圖為 ,
,
故答案為:614C; ;
;
(2)元素Y的與氫元素形成一種離子YH4+為NH4+,檢驗溶液中存在NH4+離子的方法是向溶液(或待測液)中加入NaOH溶液后加熱,能產生使濕潤的紅色石蕊試紙變藍的氣體,說明溶液中存在NH4+離子,反之,不存在NH4+離子,
故答案為:向溶液(或待測液)中加入NaOH溶液后加熱,能產生使濕潤的紅色石蕊試紙變藍的氣體,說明溶液中存在NH4+離子,反之,不存在NH4+離子;
(3)氫氧化鋁與NaOH溶液反應的離子方程式為Al(OH)3+OH-=AlO2-+2H2O,
故答案為:Al(OH)3+OH-=AlO2-+2H2O;
(4)根據元素周期律可知,氮的非金屬性強于碳,a.元素非金屬性與狀態無關,故不能證明氮的非金屬性強于碳;
b.元素的非金屬性越強,對應的最高價氧化物水化物的酸性越強,所以氮的最高價氧化物水化物的酸性比碳的最高價氧化物水化物的酸性強,能證明氮的非金屬性強于碳;
c.碳與氮形成的化合物中碳元素呈正價態,說明氮原子得電子能力大于碳原子,所以能證明氮的非金屬性強于碳,故選bc,
故答案為:N;bc;
(5)C、N、Al三種元素中,有一種元素明顯不同于其他兩種元素是Al,因為Al是金屬元素(或Al是第三周期元素),
故答案為:Al;Al是金屬元素(或Al是第三周期元素).
點評 本題考查結構性質位置關系、核外電子排布規律、元素周期律等,難度不大,推斷元素是解題關鍵,注意基礎知識的理解掌握.


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:解答題
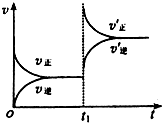 一定條件下2L的密閉容器中,反應aA(g)+bB(g)?cC(g)+dD(g)達到平衡.
一定條件下2L的密閉容器中,反應aA(g)+bB(g)?cC(g)+dD(g)達到平衡.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 698K時,向某V L的密閉容器中充入2mol H2(g)和2mol I2(g),發生反應:H2(g)+I2(g)=2HI(g)△H=-26.5kJ•mol-1,測得各物質的物質的量濃度與時間變化的關系如圖所示.
698K時,向某V L的密閉容器中充入2mol H2(g)和2mol I2(g),發生反應:H2(g)+I2(g)=2HI(g)△H=-26.5kJ•mol-1,測得各物質的物質的量濃度與時間變化的關系如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等質量的硫蒸氣和硫固體分別完全燃燒,后者放出的熱量多 | |
| B. | 由C(s,石墨)═C(s,金剛石)△H=+119 kJ•mol-1可知,金剛石比石墨穩定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若將含0.5 mol H2SO4的濃硫酸與含1 molNaOH的稀溶液混合,放出的熱量大于57.3 kJ | |
| D. | 在25℃、101 kPa時,2 g H2完全燃燒生成液態水,放出285.8 kJ熱量.則這些氫氣完成燃燒生成氣態水時,放出的熱量比285.8 kJ還要多 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗方案 | 實驗現象 |
| ①用砂紙擦后的鎂帶與沸水反應,再向反應液中滴加酚酞 | A.浮于水面,熔成小球,在水面上無定向移動,隨之消失,溶液變成紅色 |
| ②向新制的H 2S飽和溶液中滴加新制的氯水 | B.產生大量氣體,可在空氣中燃燒,溶液變成淺紅色 |
| ③鈉與滴有酚酞試液的冷水反應 | C.反應不十分劇烈,產生的氣體可以在空氣中燃燒 |
| ④鎂帶與2molL -1的鹽酸反應 | D.劇烈反應,產生的氣體可以在空氣中燃燒 |
| ⑤鋁條與2molL -1的鹽酸反應 | E.生成白色膠狀沉淀,繼而沉淀消失 |
| ⑥向氯化鋁溶液中滴加氫氧化鈉溶液 | F.生成淡黃色沉淀 |
| 實驗方案* | 實驗現象* | 有關化學方程式 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 短周期元素中,最外層電子數是其電子層數兩倍的元素共有3種 | |
| B. | 第三周期元素的離子半徑大小比較:S2->Cl->Na+>Mg2+>Al3+ | |
| C. | 日本核電站釋放出的131I、132I和133I屬于同素異形體 | |
| D. | 相同條件下,測定同濃度的Na2CO3溶液和Na2SO4溶液的pH,可比較C和S的非金屬性強弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com