
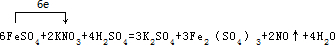 .
. 分析 n(FeSO4)=$\frac{11.4g}{152g/mol}$=0.075mol,KNO3的物質的量為0.05L×0.5mol•L-1=0.025mol,根據氧化劑、還原劑得失電子總數相等計算.
解答 解:(1)n(FeSO4)=$\frac{11.4g}{152g/mol}$=0.075mol,KNO3的物質的量為0.05L×0.5mol•L-1=0.025mol,設NO3-與NxOy中N元素化合價差為a,根據得失電子總數相等的原則,可得關系式:0.075×1=0.025×a,所以a=3即NxOy中N元素化合價為+2價,NxOy為NO,所以x=y=1,故答案為:1;1;
(2)反應生成NO,方程式為6FeSO4+2KNO3+4H2SO4=3K2SO4+3Fe2(SO4)3+2NO↑+4H2O,單線橋標出電子轉移的方向和數目可表示為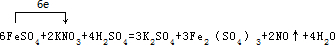 ,故答案為:
,故答案為: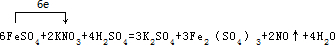 .
.
點評 本題主要考查了氧化還原反應計算,為高頻考點,側重學生的分析、計算能力的考查,明確氧化還原反應規律及基本概念是解題關鍵,注意得失電子守恒的運用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題
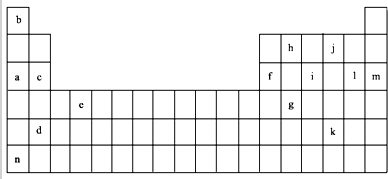
| 鋰 | X | Y | |
| 第一電離能 | 519 | 502 | 580 |
| 第二電離能 | 7296 | 4570 | 1820 |
| 第三電離能 | 11799 | 6920 | 2750 |
| 第四電離能 | 9550 | 11600 |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
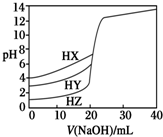 25℃時,用濃度為0.1000mol•L-1 NaOH溶液分別滴定20.00mL濃度均為0.1000mol•L-1的三種酸HX、HY、HZ,滴定曲線如圖所示.下列說法正確的是( )
25℃時,用濃度為0.1000mol•L-1 NaOH溶液分別滴定20.00mL濃度均為0.1000mol•L-1的三種酸HX、HY、HZ,滴定曲線如圖所示.下列說法正確的是( )| A. | 相同濃度時,三種酸的酸性強弱順序是:HX>HY>HZ | |
| B. | 根據滴定曲線可得,Ka(HX)=10-3 mol•L-1 | |
| C. | 滴定HY,V(NaOH)=20 mL時,c(Na+)=c(Y-)>c(OH-)=c(H+) | |
| D. | 滴定HZ,V(NaOH)=15 mL時,c(Z-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 沸點:HI>HBr>HCl>HF | |
| B. | 穩定性:NH3>PH3>AsH3(As與N位于同一主族) | |
| C. | 酸性:HClO4>H2SO4>H3PO4 | |
| D. | 堿性:NaOH>Mg(OH)2>Be(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O比Na2O2穩定 | B. | 均可與水反應生成氧氣 | ||
| C. | 均可與CO2反應 | D. | 均是典型的堿性氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 用鋁塊與氧化鐵粉末充分混和進行鋁熱反應 | |
| B. | 取少量蔗糖溶液加稀硫酸水浴加熱幾分鐘后加新制的氫氧化銅濁液加熱,觀察現象,判斷蔗糖水解的產物中是否含有葡萄糖 | |
| C. | 用稀硝酸清洗做過銀鏡反應實驗的試管 | |
| D. | 在苯中加入溴水,充分振蕩靜置,觀察現象,判斷苯環中的碳碳鍵是否存在碳碳雙鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 第Ⅰ組 | 第Ⅱ組 | 第Ⅲ組 | |
| 甲 | BaCl2 | Fe | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Zn | NaOH | MgCl2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com