
分析 (1)已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1
②N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
根據蓋斯定律:①-2×②得CH4(g)+4NO(g)═CO2(g)+2N2(g)+2H2O(l),據此計算;
(2)該反應是反應前后氣體體積減小的、放熱的可逆反應,要提高二氧化氮的轉化率,只要改變條件使化學平衡向正反應方向移動即可,依據平衡移動原理分析選項;
(3)根據平衡常數表達式結合三行式來計算物質的平衡濃度;
(4)根據反應①②③得到亞硝酸鈉、高錳酸鉀、消耗Na2S2O3之間的量的關系式為:5NO2-~2MnO4-,10Na2S2O3~5I2~2MnO4-,據此回答計算.
解答 解:(1)已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1,②N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1
根據蓋斯定律:①-2×②得CH4(g)+4NO(g)═CO2(g)+2N2(g)+2H2O(l),△H=-890.3kJ•mol-1-2×(+180kJ•mol-1)=-1250.3 kJ•mol-1;
故答案為:-1250.3 kJ•mol-1;
(2)該反應是反應前后氣體體積減小的、放熱的可逆反應,要使該反應向正反應方向移動,可改變反應物的濃度、體系的壓強、溫度等,
A、減小N02的濃度,平衡向逆反應方向移動,N02的轉化率降低,故A錯誤;
B.降低溫度,平衡向正反應方向移動,N02的轉化率提高,故B正確;
C.增加N02的濃度,相當于體系壓強增大,利于反應向正反應方向移動,N02的轉化率提高,故C正確;
D.升高溫度,平衡向逆反應方向移動,N02的轉化率降低,故D錯誤;
故答案為:BC;
(3)根據題意知平衡時:c(N2O4)=0.0120mol/L,設c(NO2)=xmol/L; K=$\frac{0.012}{{x}^{2}}$=$\frac{40}{3}$,解得x=0.03mol/L,故答案為:平衡時:c(N2O4)=0.0120mol/L,設c(NO2)=xmol/L; K=$\frac{0.012}{{x}^{2}}$=$\frac{40}{3}$,解得x=0.03mol/L,答:平衡時NO2物質的量濃度是0.03mol/;
(4)6.00mL1.0mol•L-1的高錳酸鉀標準溶液的物質的量是1.0mol/L×0.006L=0.006mol,設和碘離子反應消耗的高錳酸鉀的物質的量位n,則:
10Na2S2O3~5I2~2MnO4-,
10 2
0.1mol/L×0.02L n
n=0.0004mol,和亞硝酸鈉反應的高錳酸鉀的量是0.006mol-0.0004mol=0.0056mol,根據關系式:5NO2-~2MnO4-,得到
5NO2-~2MnO4-,
5×69 2mol
0.0056mol
所以亞硝酸鈉的質量:$\frac{0.0056mol×5×69}{2mol}$g=0.966g,所以亞硝酸鈉的質量分數為:$\frac{0.966g}{1.0g}$×100%=96.6%,
答:亞硝酸鈉的質量分數是96.6%.
點評 本題考查化學平衡計算、反應熱計算、影響化學平衡因素分析判斷、物質含量的測定等知識,注意滴定實驗的計算是難點,掌握基礎是解題關鍵,難度中等.


 芒果教輔暑假天地重慶出版社系列答案
芒果教輔暑假天地重慶出版社系列答案科目:高中化學 來源: 題型:填空題
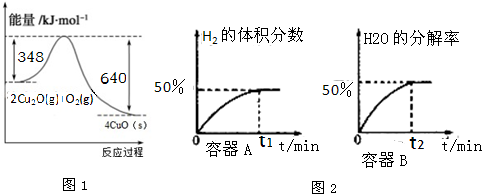
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2A在水溶液中的電離方程式為H2A=2H++A2- | |
| B. | 該溫度下,將0.01mol/L的H2A溶液稀釋20倍后溶液的pH=3 | |
| C. | 體積相同,pH均為1的鹽酸和H2A溶液分別與足量的Zn反應,產生H2較多的是H2A | |
| D. | 將0.1mol/L的H2A溶液與0.2mol/L的氨水等體積混合后,溶液中濃度最大的離子是NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
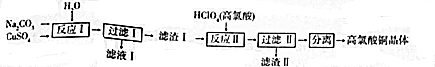
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
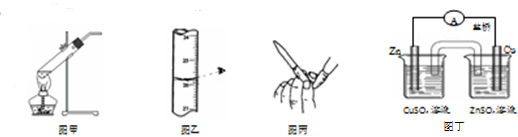
| A. | 用圖甲所示裝置加熱分解NaHCO3固體 | |
| B. | 用圖乙所示讀取滴定管讀數 | |
| C. | 用圖丙所示排堿式滴定管尖嘴內的氣泡 | |
| D. | 用圖丁所示裝置構成銅鋅原電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
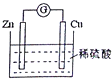
| A. | Zn片是正極 | |
| B. | 電池工作時,H+在銅片上得電子 | |
| C. | 電池工作時,電能轉變為化學能,且鋅片逐漸被消耗 | |
| D. | 電池工作時,電子從鋅片通過硫酸溶液流向銅片 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用FeCl3溶液刻制銅材電路板 | |
| B. | 用乙醇作萃取劑從碘水中提取碘 | |
| C. | 在常溫下用鋁制容器貯運濃硫酸 | |
| D. | 向含硫高的煤中加入生石灰,可減少燃料對大氣的污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:2:3 | B. | 23:24:37 | C. | 23:12:9 | D. | 36:69:92 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com