
 F2和Xe在一定條件下可生成XeF2、XeF4和XeF6三種氟化氙,它們都是極強的氧化劑(其氧化性依次遞增),都極易水解,其中:6XeF4+12H2O==2XeO3+4Xe↑ +24HF+3O2↑
F2和Xe在一定條件下可生成XeF2、XeF4和XeF6三種氟化氙,它們都是極強的氧化劑(其氧化性依次遞增),都極易水解,其中:6XeF4+12H2O==2XeO3+4Xe↑ +24HF+3O2↑
下列推測正確的是
A、XeF2分子中各原子均達到八電子結構
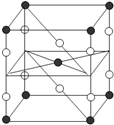
B、某種氟化氙的晶體結構單元如右圖,可推知其化學式為XeF6
C、XeF4按已知方式水解,每生成4molXe,轉移16mol電子
D、XeF2加入水中,在水分子作用下將重新生成Xe和F2
C
本題綜合考查分子結構、晶體結構、氧化還原反應及氟氣的性質,屬較難題。Xe原子本身就是8電子結構,再與F原子結合,肯定就不再是了,所以A錯;晶胞中Xe原子個數為:8×1/8+1=2,F原子個數為:8×1/4+2=4,故原子個數比Xe:F=1:2,其化學式為XeF2,B錯;由題中化學方程式可知,生成3molO2失12mol電子,生成2molXeO3失4mol電子,生成4molXe得16mol電子,所以轉移電子總數為12mol,故C正確;F2與水會劇烈反應,所以在溶液中不可能生成F2,D也錯。易錯警示:晶胞結構中質點的占有率通常采用“均攤法”,不少同學掌握不好而在此出錯。


 學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案
學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案 芒果教輔暑假天地重慶出版社系列答案
芒果教輔暑假天地重慶出版社系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 F2和Xe在一定條件下可生成XeF2、XeF4和XeF6三種氟化氙,它們都是極強的氧化劑(其氧化性依次遞增),都極易水解,其中:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑下列推測正確的是( )
F2和Xe在一定條件下可生成XeF2、XeF4和XeF6三種氟化氙,它們都是極強的氧化劑(其氧化性依次遞增),都極易水解,其中:6XeF4+12H2O═2XeO3+4Xe↑+24HF+3O2↑下列推測正確的是( )| A、XeF2分子中各原子均達到八電子結構 | B、某種氟化氙的晶體結構單元如右圖,可推知其化學式為XeF6 | C、XeF4按已知方式水解,每生成4molXe,轉移16mol電子 | D、XeF2加入水中,在水分子作用下將重新生成Xe和F2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
F2和Xe在一定條件下可生成氧化性極強且極易水解的XeF2、XeF4和XeF6三種化合物。如XeF4與水可發生如下反應:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。
下列判斷中正確的是
A.XeF2分子中各原子均達到八電子結構
B.XeF6分子中Xe的化合價為+6價
C.上述反應中氧化劑和還原劑的物質的量之比為1∶2
D.XeF4按已知方式水解,每生成4molXe,轉移12mol電子
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省五校高三第一次聯考化學試卷 題型:選擇題
F2和Xe在一定條件下可生成氧化性極強且極易水解的XeF2、XeF4和XeF6三種化合物。如XeF4與水可發生如下反應:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。
下列判斷中正確的是
A.F一般無正價,但在HFO中的F價態為+1
B.XeF2分子中各原子均達到8電子結構
C.XeF4按已知方式水解,反應中氧化劑為XeF4、還原劑為H2O
D.XeF4按已知方式水解,每生成4molXe,轉移16mol電子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com