
| 實驗變量 實驗序號 | 銀氨溶液量 (ml) | 乙醛的量 (滴) | 水浴溫度 (℃) | 反應混合液PH | 出現銀鏡時間(min) |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
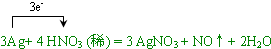 ,
,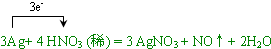 ;
;

科目:高中化學 來源: 題型:
| A、2FeCl3(aq)+2KI(aq)═2FeCl2(aq)+2KCl(aq)+I2(aq)△H<0 |
| B、Ba(OH)2?8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3?H2O(aq)+8H2O(l)△H>0 |
| C、4Al(s)+6H2O(l)+3O2(g)═4Al(OH)3(s)△H<0 |
| D、Zn(s)+2MnO2(s)+2H2O(l)═2MnOOH(s)+Zn(OH)2(s)△H<0 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
2- 4 |
| H+ |
2- 7 |
| 電解 |
| 還原 |
| 沉淀 |

查看答案和解析>>
科目:高中化學 來源: 題型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化學 來源: 題型:
 下面的各方框表示有關的一種反應物或生成物(某些物質已經略去),其中常溫下A、C、D為無色氣體,B為液體,C能使濕潤的紅色石蕊試紙變藍.A、B、C的物質的量之比為1:1:1.
下面的各方框表示有關的一種反應物或生成物(某些物質已經略去),其中常溫下A、C、D為無色氣體,B為液體,C能使濕潤的紅色石蕊試紙變藍.A、B、C的物質的量之比為1:1:1.查看答案和解析>>
科目:高中化學 來源: 題型:
| A | B | C | |
| D | E | F |
| A、D的單質是常見的半導體材料 |
| B、B與E形成的化合物不只一種 |
| C、C與F的原子序數之差一定為8 |
| D、C屬于鹵族元素,對應的單質能與水反應生成兩種酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:
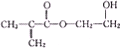 甲基丙烯酸烴乙酯是一種有機合成中重要的原料,其結構簡式如圖所示,下列有關說法錯誤的是( )
甲基丙烯酸烴乙酯是一種有機合成中重要的原料,其結構簡式如圖所示,下列有關說法錯誤的是( )| A、能發生加成反應 |
| B、能發生取代反應 |
| C、一定條件下,能與乙醇發生酯化反應 |
| D、既能是溴水褪色,又能使酸性高猛酸鉀溶液褪色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com