
分析 (1)鉀與四氟化硅反應生成硅和氟化鉀;
(2)①依據反應4Al+3K2SiF6$\frac{\underline{\;高溫\;}}{\;}$3Si+2KAlF4+2K2AlF5,各種元素化合價變化解答;
②鎂與二氧化硅反應生成硅和氧化鎂,依據原子個數守恒判斷產物,寫出化學方程式;
③晶體硅和無定形硅為同素異形體,二者結構不同,性質不同;
(3)Si和FeO反應生成Fe和二氧化硅;
(4)依據原子個數守恒寫出化學方程式;
(5)一氧化硅具有絕緣性,用電解法對硅表面處理生成SiO薄膜時,硅發生氧化反應生成一氧化硅.
解答 解:(1)瑞典化學家貝采尼烏斯用金屬鉀還原SiF4獲得單質硅,反應的化學方程式為:4K+SiF4═Si+4KF,故答案為:4K+SiF4═Si+4KF;
(2)①在反應4Al+3K2SiF6$\frac{\underline{\;高溫\;}}{\;}$3Si+2KAlF4+2K2AlF5,鋁元素化合價升高,硅元素化合價降低,所以鋁做還原劑,K2SiF6做氧化劑,硅為還原產物,KAlF4和2K2AlF5為還原產物,反應3mol鋁轉移12mol電子,生成84g硅,所以每轉移6NA電子,得到42g Si,Al元素在KAlF4和K2AlF5中化合價都是+3價,
故答案為:AC;
②鎂與二氧化硅反應生成硅和氧化鎂,方程式為:2Mg+SiO2$\frac{\underline{\;高溫\;}}{\;}$Si+2MgO,
故答案為:2Mg+SiO2$\frac{\underline{\;高溫\;}}{\;}$Si+2MgO;
③晶體硅和無定形硅為同素異形體,二者結構不同,物理性質和化學性質可能存在較大差別,
故答案為:結構決定性質,當結構不同時,物質的物理性質和化學性質可能存在較大差別;
(3)Si和FeO反應生成Fe和二氧化硅,反應的化學方程式為Si+2FeO$\frac{\underline{\;高溫\;}}{\;}$SiO2+2Fe,
故答案為:Si+2FeO$\frac{\underline{\;高溫\;}}{\;}$SiO2+2Fe;
(4)硅粉與干燥的Ca(OH)2和NaOH混合,并加強熱,即可迅速得到H2、Na2SiO3、CaO,依據原子個數守恒,轉移電子數守恒可得反應的化學方程式為:Si+2NaOH+Ca(OH)2=Na2SiO3+CaO+2H2↑;
故答案為:Si+2NaOH+Ca(OH)2=Na2SiO3+CaO+2H2↑;
(5)一氧化硅具有絕緣性,用電解法對硅表面處理生成SiO薄膜時,硅發生氧化反應生成一氧化硅,作陽極,故答案為:絕緣性;陽.
點評 本題考查了硅及其化合物的性質、原電池原理的應用,側重于元素化合物知識的綜合理解和運用的考查,熟悉硅及其化合物的性質、氧化還原反應的規律、原電池原理是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
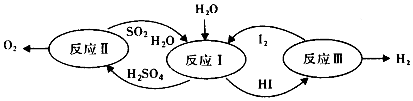
| A. | 設計該循環是為了制取能源氣體O2 | |
| B. | 整個循環過程中產生1mol O2的同時產生1molH2 | |
| C. | 圖中反應Ⅰ、Ⅱ、Ⅲ均可在常溫常壓下進行 | |
| D. | 圖中反應Ⅰ、Ⅱ、Ⅲ均為氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 231.5mL | B. | 268.8mL | C. | 287.5mL | D. | 313.6mL |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D |
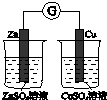 | 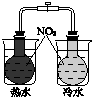 | 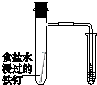 | 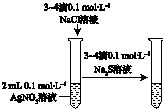 |
| 驗證化學能轉化為電能 | 證明溫度對平衡移動的影響 | 驗證鐵發生析氫腐蝕 | 驗證AgCl溶解度小于Ag2S |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 糖類和蛋白質都是人體重要的營養物質 | |
| B. | 蛋白質在一定條件下能發生水解反應,生成氨基酸 | |
| C. | 加熱能殺死甲型H1N1流感病毒,因為病毒的蛋白質受熱變性 | |
| D. | 蛋白質溶液中加入飽和硫酸銨溶液,蛋白質析出,如再加水也不溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅的金屬活潑性比鐵的差,可在海輪外殼上裝若干銅塊以減緩其腐蝕 | |
| B. | 明礬能水解生成Al(OH)3膠體,可用作水的消毒劑 | |
| C. | FeCl3溶液能與Cu反應,可用于蝕刻印刷電路 | |
| D. | 氯化鋁是一種電解質,可用于電解法制鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ca2+、K+、Cl-、S2-四種離子的半徑依次減小 | |
| B. | 熔融的NaHSO4中陰陽離子的數目比為1:2 | |
| C. | 氫化鋰三兄弟--LiH、LiD、LiT三種物質的質子數之比為4:5:6 | |
| D. | 一個乙醛分子中存在7對共用電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高純硅是工業上制造光導纖維的主要原料 | |
| B. | 開發和推廣新能源汽車是實現低碳生活的途徑之一 | |
| C. | 尋找高效催化劑,利用太陽能分解水是制取氫氣的較理想方法 | |
| D. | 不需要通過化學反應就能從海水中獲得淡水 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com