
| A. | AlCl3溶液與燒堿溶液反應,當n(OH-):n(Al3+)=7:2時,2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O | |
| B. | CuCl2溶液與NaHS溶液反應,當n(CuCl2):n(NaHS)=1:2時,Cu2++2HS-═CuS↓+H2S↑ | |
| C. | Cl2與FeBr2溶液反應,當n(Cl2):n(FeBr2)=1:1時,2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | Fe與稀硝酸反應,當n(Fe):n(HNO3)=1:2時,3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O |
分析 A.AlCl3溶液與燒堿溶液反應,當n(OH-):n(Al3+)=7:2時反應生成氫氧化鋁沉淀和偏鋁酸鈉和水;
B.CuCl2溶液與NaHS溶液反應,當n(CuCl2):n(NaHS)=1:2時反應生成硫化銅沉淀和硫化氫;
C.Cl2與FeBr2溶液反應,當n(Cl2):n(FeBr2)=1:1時,二價鐵離子全部被氧化,溴離子只氧化一半;
D.Fe與稀硝酸反應,當n(Fe):n(HNO3)=1:2時,硝酸不足,反應生成硝酸亞鐵、一氧化氮和水;
解答 解:A.AlCl3溶液與燒堿溶液反應,當n(OH-):n(Al3+)=7:2時,離子方程式,2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O,故A正確;
B.CuCl2溶液與NaHS溶液反應,當n(CuCl2):n(NaHS)=1:2時,離子方程式:Cu2++2HS-═CuS↓+H2S↑,故B正確;
C.氯氣先氧化亞鐵離子后氧化溴離子,發生反應Cl2+2Fe2+=2Cl-+2Fe3+、Cl2+2Br-=Br2+2Cl-,當n(Cl2):n(FeBr2)=1:1時,假設二者都是2mol,則亞鐵離子完全被氧化需要1mol氯氣、剩余1mol氯氣氧化2mol溴離子,所以還有一半溴離子未被氧化,則離子方程式為2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-,故C錯誤;
D.Fe與稀硝酸反應,當n(Fe):n(HNO3)=1:2時,離子方程式:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O,故D正確;
故選:C.
點評 本題考查了離子方程式的書寫,側重考查反應物用量有關的離子反應的方程式書寫,明確反應實質是解題關鍵,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ),它能與Fe2+形成紅色配合物(如圖1),該配離子中Fe2+與氮原子形成配位鍵共有6個.
),它能與Fe2+形成紅色配合物(如圖1),該配離子中Fe2+與氮原子形成配位鍵共有6個.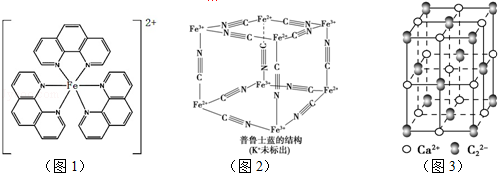
 .已知CaC2晶體密度為ag•cm-3,NA表示阿伏加德羅常數,則CaC2晶胞體積為$\frac{256}{a{N}_{A}}$cm3.
.已知CaC2晶體密度為ag•cm-3,NA表示阿伏加德羅常數,則CaC2晶胞體積為$\frac{256}{a{N}_{A}}$cm3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
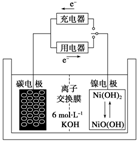 一種碳納米管能夠吸附氫氣,用這種材料制備的二次電池原理如圖所示,該電池的電解質為6mol•L-1KOH溶液,下列說法中正確的是( )
一種碳納米管能夠吸附氫氣,用這種材料制備的二次電池原理如圖所示,該電池的電解質為6mol•L-1KOH溶液,下列說法中正確的是( )| A. | 放電時K+移向碳電極 | |
| B. | 放電時離子交換膜每通過4mol離子,碳電極質量減少12g | |
| C. | 放電時電池正極的電極反應為NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| D. | 該電池充電時將鎳電極與電源的負極相連 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 微粒 | EO2- | EO3- |
| 立體構型名稱 |
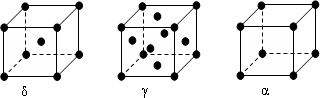
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 燃料的使用和防污染是社會發展中一個無法回避的矛盾話題.
燃料的使用和防污染是社會發展中一個無法回避的矛盾話題.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 將溶液 的c(H+)、c(OH-)之比取為AG[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$].25℃時,用0.01mol.L-1的氫氧化鈉溶液滴定20ml相同物質的量濃度的醋酸溶液,滴定曲線如圖所示.下列有關敘述正確的是( )
將溶液 的c(H+)、c(OH-)之比取為AG[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$].25℃時,用0.01mol.L-1的氫氧化鈉溶液滴定20ml相同物質的量濃度的醋酸溶液,滴定曲線如圖所示.下列有關敘述正確的是( )| A. | A點時c(CH3COO-)>c(Na+) | |
| B. | 室溫時0.01mol.L-1的醋酸溶液pH=6 | |
| C. | OA段溶液中均有:c(CH3COO-)>c(CH3COOH) | |
| D. | 若B點時加入NaOH溶液40mL,所得溶液中:c(CH3COO-)+2c(CH3COOH)=c(OH-)-c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
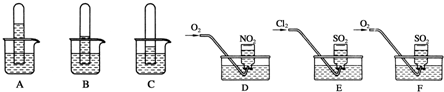
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com